“与儿童相比,ALL 成人的预后要差得多,大约一半的 B-ALL 成人会在目前可用的疗法中复发,”医学博士、ZUMA-3 研究员和医学肿瘤学家、坦帕莫菲特癌症中心的 Bijal Shah 说,佛罗里达。“我们现在对这些患者的治疗有了新的有意义的进步。Tecartus 的单次输注已显示出持久的反应,表明长期缓解的潜力和一种新的护理方法。”
该批准基于 ZUMA-3 的结果,这是一项全球性、多中心、单臂、开放标签研究,其中 65% 的可评估患者(n=54)达到完全缓解(CR)或血液学恢复不完全的 CR( CRi) 的中位实际随访时间为 12.3 个月。超过一半的患者的 CR 持续时间估计超过 12 个月。在疗效可评估的患者中,中位缓解持续时间 (DOR) 为 13.6 个月。在接受目标剂量 Tecartus 治疗的患者 (n=78) 中,3 级或更高级别的细胞因子释放综合征 (CRS) 和神经系统事件分别发生在 26% 和 35% 的患者中,并且通常得到良好管理。
Kite 首席执行官 Christi Shaw 表示:“今天标志着 Kite 在不到四年的时间里获得 FDA 批准的第四个细胞治疗适应症,这表明我们致力于为许多不同血液系统恶性肿瘤的患者推进 CAR T。“Tecartus 已经改变了成人套细胞淋巴瘤患者的治疗结果,我们期待为 ALL 患者带来治愈的希望。”
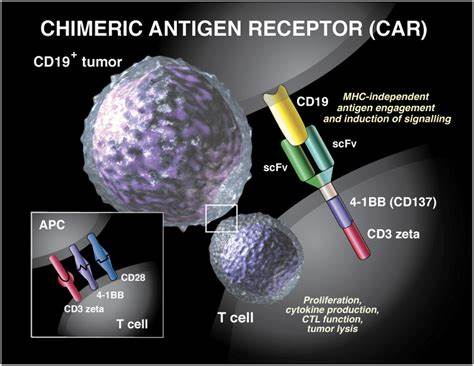
患有复发性或难治性 ALL 的成人经常接受多种治疗,包括化疗、靶向治疗和干细胞移植。CAR T 细胞疗法的作用不同,它利用患者自身的免疫系统来对抗癌症。使用 CAR T,抽取患者的血液并分离 T 细胞。然后用特定受体对 T 细胞进行基因工程改造,使它们能够识别和攻击癌细胞,并将其放回患者体内。
白血病和淋巴瘤协会 (LLS) 首席科学官 Lee Greenberger 博士说:“大约一半的 ALL 病例实际上发生在成人身上,与儿科 ALL 不同,成人 ALL 历来预后不佳。” “开发能够改变癌症患者生活的新疗法一直是 LLS 的梦想。我们很自豪地看到 CAR T 的潜力在获得 brexucabtagene autoleucel 的批准后为更多人实现。”
Tecartus 目前也在欧盟和英国接受审查,用于治疗患有复发性或难治性 B 细胞前体 ALL 的成年患者。

 购物车
购物车