土耳其 Infliximab for Injection 英夫利西单抗 100mg remlcade 100mg
类风湿关节炎,克罗恩病,瘘管性克罗恩病,强直性脊柱炎,银屑病,成人溃疡性结肠炎
| 数量: | 库存 50 件 |
主要成份:英夫利西单抗
辅料:蔗糖、吐温80、磷酸二氢钠(或磷酸二氢钠一水合物)、磷酸氢二钠(或磷酸氢二钠一水合物)
类风湿关节炎
本品是疾病控制性抗风湿药物。对于中重度活动性类风湿关节炎患者,本品与甲氨蝶吟合用可用于:
·减轻症状和体征;
·改善身体机能,预防患者残疾。
成人及6岁以上儿童克罗恩病
本品可用于对于接受传统治疗效果不佳的中重度活动性克罗恩病的成人和6岁及以上的儿童患者,用于:
·减轻症状和体征;
·诱导并维持临床缓解;
·诱导成人患者的粘膜愈合;
·改善生活质量;
·使成人患者减少皮质激素用量或停止使用皮质激素。
瘘管性克罗恩病
对于瘘管性克罗恩病患者,本品可用于:
·减少肠-皮肤瘘管和直肠-阴道瘘管的数量,促进并维持瘘管愈合;
·减轻症状和体征:
·改善生活质量。
强直性脊柱炎
对于活动性强直性脊柱炎患者,本品可用于:
·减轻症状和体征,包括增加活动幅度;
·改善身体机能;
·改善生活质量。
银屑病
本品用于需系统治疗且对环砲霉素、甲氨蝶吟或光化学疗法等其它系统治疗无效、禁忌或不耐受的慢性重度斑块型银屑病成年患者。本品仅用于能在医师的密切监测下进行治疗并由医生进行定期随访的患者。
成人溃疡性结肠炎
对于接受传统治疗效果不佳、不耐受或有医学禁忌的中重度活动性溃疡性结肠炎成年患者,本品可用于:减轻症状和体征、诱导并维持临床缓解和粘膜愈合、使患者减少或停止使用糖皮质激素。
溃疡性结肠炎,6岁或以上:
首次5mg/kg静脉滴注,第0、2、6周及之后每8周给予相同剂量各1次。
银屑病关节炎:
首次5mg/kg静脉滴注,第0、2、6周及之后每8周给予相同剂量各1次治疗银屑病关节炎
用法:静脉输注。
用量:
类风湿关节炎
首次给予本品3mg/kg,然后在首次给药后的第2周和第6周及以后每隔8周各给予一次相同剂量。本品应与甲氨蝶吟合用。对于疗效不佳的患者,可考虑将剂量调整至10mg/kg,和/或将用药间隔调整为4周。
成人中重度活动性克罗恩病、瘘管性克罗恩病
首次给予本品5mg/kg,然后在首次给药后的第2周和第6周及以后每隔8周各给予一次相同剂量。对于疗效不佳的患者,可考虑将剂量调整至10mg/kg。
儿童中重度活动性克罗恩病(6至17岁)
首次给予本品5mg/kg,然后在首次给药后的第2周和第6周及以后每隔8周各给予一次相同剂量。现有数据不支持在治疗最初10周内未产生应答的儿童和青少年中继续给予本品治疗。
某些患者可能需要一个更短的给药间隔以维持其临床获益,而对于另一些患者而言延长给药间隔也可以产生足够的临床获益。增加剂量至超过5mg/kg,每8周给予一次的儿童克罗恩病患者发生不良反应的风险可能升高。对于剂量调整后没有获得更多治疗获益的患者,应仔细考虑是否釆用调整后的剂量继续治疗。
本品的安全性和疗效尚未在6岁以下克罗恩病患儿中进行研究。目前现有的药代动力学数据在药代动力学特征中进行了介绍,但无法对6岁以下儿童给出用法用量建议。
强直性脊柱炎
首次给予本品5mg/kg,然后在首次给药后的第2周和第6周及以后每隔6周各给予一次相同剂量。
斑块型银屑病
首次给予本品5mg/kg,然后在首次给药后的第2周和第6周及以后每隔8周各给予一次相同剂量。若患者在第14周后(即4次给药后)没有应答,不应继续给予本品治疗。
银屑病患者再次给药
银屑病患者相隔20周后再次单次给药的经验有限,与最初的诱导治疗相比,提示本品的有效性降低,且轻到中度输液反应增加。
疾病复发后,有限的反复诱导治疗经验表明,与8周维持治疗相比,输液反应增加(包括严重反应)。
如维持治疗中断,不推荐再次启动诱导治疗,应按照维持治疗再次给药。
成人溃疡性结肠炎
首次给予本品5mg/kg,然后在首次给药后的第2周和第6周及以后每隔8周各给予 一次相同剂量。
输液反应用药说明
本品静脉给药时间不得少于2小时。接受本品给药的所有患者应在输注后至少观察1~2小时,以观察急性输液相关反应。医院需配备肾上腺素、抗组胺药、糖皮质激素及人工气道等急救物品。
根据医生判断,患者可接受如抗组胺药、氢化可的松和/或对乙酰氨基酚预处理,同时降低输注速度,以减少输液相关反应的风险,特别是对于以前曾发生过输液相关反应的患者更应慎重。
输液期间,可以通过减慢输液速度或者暂停输液来改善轻中度输液反应,一旦反应得到缓解,可以按照较低的输液速度重新开始输液,和/或给予抗组胺药、对乙酰氨基酚和/或糖皮质激素等治疗性药物。对于经过上述干预后仍无法耐受药物输注的患者,应立即停药。
输液期间或输液后,对于出现重度输液相关性超敏反应的患者,应停止本品治疗。根据所岀现的输液反应的症状和体征对重度输液反应进行处理。应配备适当的人员和药物,以备发生过敏反应时给予及时的治疗。
使用指导
应进行无菌操作。
计算剂量,确定本品的使用瓶数:本品每瓶含英夫利西单抗100mg,计算所需配制的本品溶液总量。
使用配有21号(0.8mm)或更小针头的注射器,将每瓶药品用10ml无菌注射用水溶解:除去药瓶的翻盖,用医用酒精棉签擦拭药瓶顶部,将注射器针头插入药瓶胶盖,将无菌注射用水沿着药瓶的玻璃壁注入。如药瓶内的真空状态己被破坏,则该瓶药品不能使用。轻轻旋转药瓶,使药粉溶解。避免长时间或用力摇晃,严禁振荡。溶药过程中可能出现泡沫,放置5分钟后,溶液应为无色或淡黄色,泛乳白色光。由于英夫利西单抗是一种蛋白质,溶液中可能会有一些半透明微粒。如果溶液中出现不透明颗粒、变色或其它物质,则不能继续使用。
用0.9%氯化钠注射液将本品的无菌注射用水溶液稀释至250ml:从250ml 0.9%氯化 钠注射液瓶或袋中抽出与配制的本品溶液总量相同的液体量,之后,将配置好的本品溶液总量全部注入该输液瓶或袋中,轻轻混合。最终获得的输注溶液浓度范围应在0.4mg/ml至4mg/ml之间。请勿使用其他溶剂对本品溶液进行稀释。
本品输注应在复溶并稀释后3小时内进行。输液时间不得少于2小时:输液装置上应配有一个内置的、无菌、无热原、低蛋白结合率的滤膜(孔径<1.2um)。本品不含抗菌防腐剂,未用完的输液不应再贮存使用。
未进行本品与其它药物合用的物理生化兼容性研究,本品不应与其它药物同时进行输液。
经胃肠道外给药的产品在给药前应目检是否存在微粒物质或变色现象。如果发现存在不透明颗粒、变色或其它异物,则该药品不可使用。
临床试验中报告的最常见的药物不良反应(ADR)是上呼吸道感染,英夫利西单抗组与对照组的发生率分别为25.3%和16.5%0与包括本品在内的TNF抑制剂使用有关的最严重的药物不良反应包括乙型肝炎病毒(HBV)再激活、充血性心力衰竭(CHF)、严重感染(包括脓毒症、机会性感染和结核病)、血清病(迟发性超敏反应)、血液系统反应、系统性红斑狼疮/狼疮样综合征、脱髓鞘性疾病、肝胆事件、淋巴瘤、肝脾T细胞淋巴瘤(HSTCL)、白血病、Merkel细胞癌、黑色素瘤、儿童恶性肿瘤、结节病/肉瘤样反应、肠道或肛周脓肿(在克罗恩病中)和严重的输液反应。
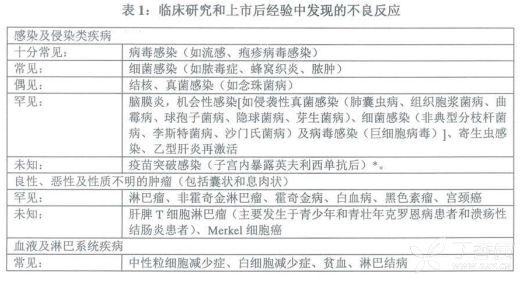
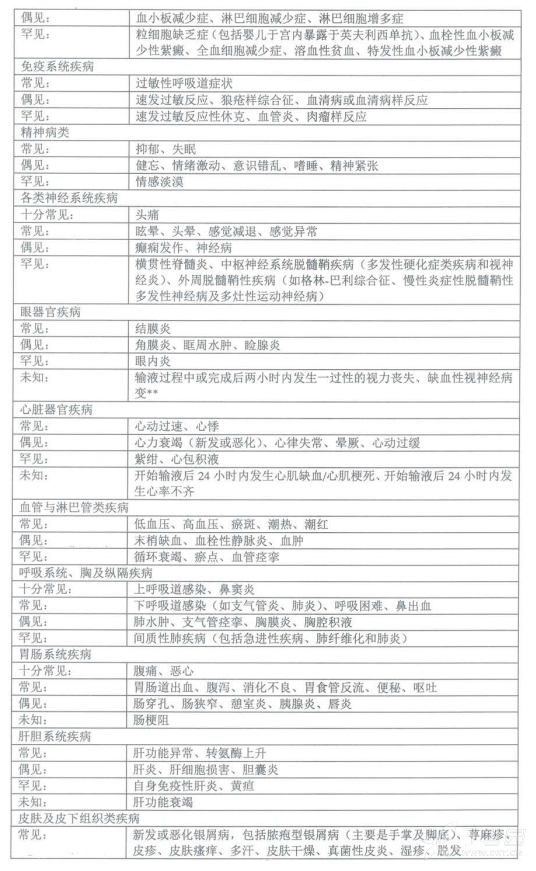
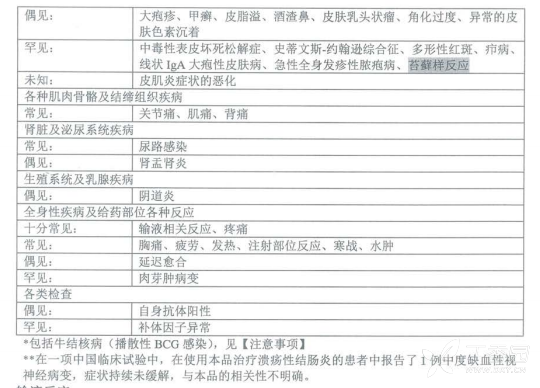
表1列出了基于临床研究及上市后经验的药物不良反应(其中一些为致死性病例)。在器官系统分类内,根据发生频率将不良反应分类如下:十分常见(>1/10);常见(>1/100,<1/10);偶见(>1/1000,<1/100):罕见(>1/10000,<1/1000);十分罕见(<1/10000);未知(无法从现有数据估算)。在每个频率组中,不良反应按严重程度以降序排列。
输液反应
输液相关反应在临床试验中被界定为输液过程中或输液后1小时内发生的任何不良事件。在III期临床试验中,输液中和输液结束后的1小时内,英夫利西单抗组和安慰剂组患者的输液相关反应发生率分别为18%与5%0在诱导期发生输液反应的英夫利西单抗组患者中有27%的患者在维持期也发生了输液反应。而在诱导期未发生输液反应的患者中9%的患者在维持期发生了输液反应。
在所有的本品输注中,3%的患者会伴随出现发热或寒战等非特异性症状,1%的患者伴随出现心肺反应(主要表现为胸痛、低血压、高血压或呼吸困难),低于1%的患者伴随出现瘙痒、奪麻疹,或同时出现瘙痒/尊麻疹症状及心肺反应。低于1%的患者出现了严重输液反应,包括:过敏反应、惊厥、红斑和低血压。约3%的患者因与输液相关的反应而中断治疗。所有发生上述反应的患者经过治疗和/或停止输液后均康复。总体上多次药物输注并不会使上述事件的发生率增加。在银屑病研究I(EXPRESS)中,输液反应发生率在银屑病患者一年的治疗中保持稳定。在银屑病研究II(EXPRESS II)中,发生率随时间有所变化,最终输液后的发生率略高于最初输液后。在3项银屑病研究中,导致输液反应的输注占总输注次数的百分比(即1小时内发生的不良事件)在3mg/kg组是7%,5mg/kg组是4%,安慰剂组是1%。
与阴性患者相比,英夫利西单抗抗体呈阳性的患者更可能(大约2~3倍)出现输液反应。合并使用免疫抑制剂显示会降低英夫利西单抗抗体的出现以及输液反应发生率。
在一项类风湿关节炎临床试验(ASPIRE)中,最初3次输液时间超过2小时,未发生严重输液反应的患者后续输液时间可缩短,但不短于40分钟。该试验中66%(1040名中有686名)的患者至少接受过一次不超过90分钟的短时间输注,44%(1040名中有454名)的患者至少接受过一次不超过60分钟的短时间输注。至少接受过一次短时间输注的英夫利西单抗组有15%(74/494)的患者发生了输液反应,0.4%(2/494)的患者发生了严重输液反应。尚未进行剂量大于6mg/kg的短时间输注研究。
克罗恩病患者临床研究(SONIC)中,英夫利西单抗单药治疗患者的输液相关反应发生率为16.6%(27/163),英夫利西单抗与硫唑嘌呤(AZA)合用患者与AZA单用患者的输液相关反应发生率分别为5%(9/179)和5.6%(9/161)。英夫利西单抗单用患者中发生1例严重输液反应(<1%)。
上市后监测中,有与使用本品相关的类似速发过敏反应的报告,包括喉水肿、咽部水肿、重度支气管痉挛和惊厥发作。在输注英夫利西单抗的过程中或2小时内,己有瞬时性视觉丧失的报道。己有开始本品输注后24小时内脑血管意外、心肌缺血/梗死(有些是致命的)和心率不齐发生的报道。
再次给药后的输液反应
在类风湿关节炎、克罗恩病和银屑病临床试验中,停药一段时间后再次给予本品输液反应的发生率高于常规的维持治疗。
一项在中重度银屑病患者中进行的临床试验评价了本品长期维持治疗与诱导治疗后再次给予本品治疗的疗效和安全性(最多输注4次,分别在第0、2、6和14周)。试验中,间歇给药组中4%(8/219)的患者发生严重输液反应,而维持治疗组只有<1%(1/222)的患者发生严重输液反应。入组本试验的患者不接受任何免疫抑制剂的合并治疗。间歇给药组定义为诱导治疗(最多在第0、2、6和14周4次输注)后,经过一段时间无治疗,根据疾病的复发再次给予本品。本试验中,主要的严重输液反应发生在第2周的第2次输注。症状包括但不仅限于呼吸困难、專麻疹、面部浮肿和低血压。在这些病例中,停止本品治疗和/或使用其它疗法后体征和症状完全消退。
迟发性超敏反应
临床试验中迟发性超敏反应不常见,且发生在本品停药期间不足一年的患者中。银屑病研究中,大约1%的本品治疗组患者出现了退发性超敏反应,该反应发生于治疗早期。症状和体征包括肌肉疼痛和/或关节痛、出现发热和/或皮疹,部分患者出现皮肤瘙痒、面部水肿、手或唇水肿、吞咽困难、尊麻疹、喉痛和头痛。
本品停药间期超过一年的迟发性超敏反应发生率数据不充足,但有限的临床研究显示,随着本品停药间期的延长,迟发性超敏反应风险增高。
为期一年的临床研究中,克罗恩病患者重复输液(ACCENTI)的血清病样反应发生率为2.4%。
免疫原性
使用本品治疗时可能会出现英夫利西单抗抗体。测量患者样本中英夫利西单抗抗体所用的检测方法可能会受到血清中英夫利西单抗的干扰,从而低估患者抗体发生率。
在接受3剂诱导方案治疗后进行维持用药1~2年的患者中,英夫利西单抗抗体的发生率大约是10%。在经过>16周的无药期后接受本品治疗的克罗恩病患者中,观察到英夫利西单抗抗体的发生率增高。在一项银屑病关节炎研究中,有191名患者在使用或不使用甲氨蝶吟(MTX)的情况下接受了5mg/kg剂量用药。结果显示,15%的患者出现了英夫利西单抗抗体,大多数抗体呈阳性的患者其滴度较低,与抗体阴性患者相比,抗体阳性患者更可能具有较高的清除率,因而可能降低疗效,出现输液反应。在接受6-巯基嘌呤/硫唑嘌呤(6-MP/AZA)或MTX等免疫抑制剂治疗的类风湿关节炎和克罗恩病患者中,抗体的出现较少见。
银屑病研究II包括了5mg/kg和3mg/kg剂量组,在按照5mg/kg剂量、每8周用药一次进行了一年治疗的患者中,观察到36%的患者产生抗体;在按照3mg/kg剂量、每8周用药一次进行了一年治疗的患者中,这一比例是51%。银屑病研究III(SPIRIT)也包括了5mg/kg和3mg/kg剂量组,在按照5mg/kg剂量诱导方案(0、2和6周)进行治疗的患者中,观察到20%的患者产生抗体;在按照3mg/kg剂量进行诱导治疗的患者中,这一比例是27%。虽然抗体形成增多,但银屑病研究I和研究II中(按照5mg/kg剂量进行诱导治疗之后每8周一次进行为期一年的维持治疗的患者)以及银屑病研究III(按照5mg/kg剂量进行诱导治疗的患者)中患者输液反应的发生率(14.1%~23.0%)和严重输液反应的发生率(<1%)与在其它研究人群中观察到的比例近似。银屑病患者与其它疾病患者相比,在长期接受本品治疗后,尚不知免疫原性的增高是否对疗效以及输液反应发生率有影响。
感染
在接受本品治疗的患者中曾观察到有结核、包括脓毒症和肺炎的细菌感染、侵袭性真菌感染、病毒感染和其它机会性感染,其中部分感染是致命的。死亡率超过5%的最常报告的机会性致病菌感染包括肺囊虫病、念珠菌病、李斯特菌病和曲霉病。
在临床研究中,英夫利西单抗组患者的感染率为36%,安慰剂组患者的感染率为25%。
在类风湿关节炎临床试验中,英夫利西单抗与甲氨蝶吟合用组患者严重感染发生率(包括肺炎)高于甲氨蝶吟单用组,剂量在6mg/kg或以上时更为突出。
上市后自发报告中,最常见的严重不良事件为感染,部分为致死性病例。近50%的死亡报告与感染相关。己报告的结核病例包括粟粒性结核和肺外结核。
肝胆系统
根据本品上市后经验,己有黄疸和非传染性肝炎(其中一些具有自身免疫性肝炎的特征)病例的报告。
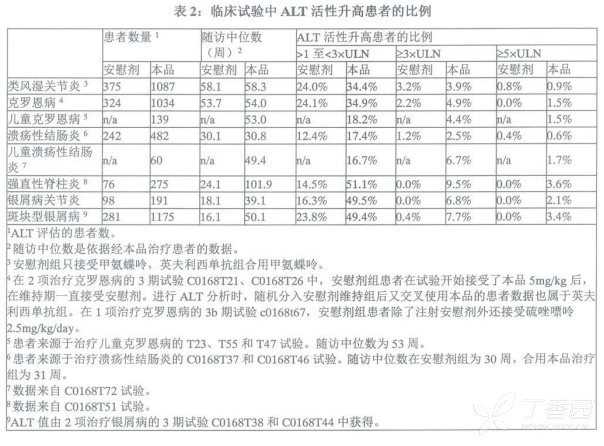
在临床试验中,观察到了使用本品的患者出现轻度或中度谷丙转氨酶(AET)和谷草转氨酶(AST)升高,但未导致重度肝损伤。ALT升高至正常范围上限(ULN)的5倍或以上(见表2)。英夫利西单抗组(单用或与其它免疫抑制剂合用)患者转氨酶(ALT比AST更常见)升高比例高于对照组(见表2)。大多数转氨酶异常是一过性的,但少数患者转氨酶升高的时间较长。一般情况下,ALT和AST升高的患者均未出现症状,在继续使用本品、停用本品或调整合并用药后,该异常现象可减轻或消除。
恶性肿瘤和淋巴增生性疾病
英夫利西单抗临床治疗中,5780例患者(5494患者-年)中发现5例淋巴瘤和26例非淋巴瘤恶性肿瘤,而安慰剂组的1600例患者(941患者-年)发现1例非淋巴瘤恶性肿瘤,无淋巴瘤。
在长达5年的英夫利西单抗长期安全性随访研究中,3210例患者(6234患者-年)报告了5例淋巴瘤和38例非淋巴瘤恶性肿瘤。
上市后用药经验中报告了包括淋巴瘤的恶性肿瘤病例。
在一项中重度慢性阻塞性肺病(COPD)探索性临床研究中(现吸烟者或有吸烟史患者),本品给药剂量类似于类风湿关节炎和克罗恩病成人患者的治疗剂量,9例发生恶性肿瘤(包括1例淋巴瘤),随访期中位值为0.8年[发生率5.7%(95%置信区间2.65%~10.6%)]。对照组77例患者中有1例恶性肿瘤报告,随访期中位值为0.8年[发生率1.3%(95%置信区间0.03%~7.0%)]。大多数恶性肿瘤为肺癌或头颈部癌。一项基于人群的回顾性队列研究发现,与未接受过生物制剂组或普通人群(包括60岁以上)相比,使用英夫利西单抗的类风湿性关节炎女性患者中宫颈癌的发生率升高。
此外,上市后使用本品所报告的肝脾T细胞淋巴瘤病例绝大多数发生在克罗恩病或溃疡性结肠炎患者中,且大多数为青少年或青年男性。
抗核抗体(ANA)/抗双链脱氧核糖核酸(dsDNA)抗体
临床试验中,基线时抗核抗体(ANA)阴性的英夫利西单抗组患者约有一半在治疗中ANA呈阳性,此现象在安慰剂组患者中的发生率约为20%。在英夫利西单抗组患者中抗dsDNA抗体的转阳率约为17%,而在安慰剂组患者中为0%。少见狼疮及狼疮样综合征的报告。
充血性心力衰竭
在中重度心力衰竭[纽约心脏学会心功能分级(NYHAIII/IV)级,且左心室射血分数<35%[患者参加的临床试验中,有150名患者随机分为英夫利西单抗10mg/kg、5mg/kg或安慰剂组,在第0、2和6周接受三次药物输注。结果显示,在接受10mg/kg剂量本品治疗的患者中观察到了较高的死亡率,且因心力衰竭导致的住院发生率增高。到一年时,8名10mg/kg本品组患者死亡,5mg/kg本品组和安慰剂组各有4名患者死亡。与安慰剂组相比,在10mg/kg和5mg/kg本品治疗组中,发生呼吸困难、低血压、心绞痛和头晕的几率有增高的趋势。尚未在轻度心力衰竭(NYHA分类I/II)患者中进行本品研究。
上市后经验显示,使用本品的患者(无论有无明显诱发因素)有心力衰竭加重的报告。
已有初发性心力衰竭(包括无已知既往心血管疾病的患者出现的心力衰竭)报告,其中一些患者的年龄在50岁以下。
儿童克罗恩病患者的不良反应
总体上,接受本品治疗的儿童克罗恩病患者发生的不良事件的频率和类型与成人克罗恩病患者类似。以下段落描述了与成人之间的差异及其他特殊考虑事项。
在103例随机接受本品5mg/kg(截至54周)治疗的儿童克罗恩病患者中,以下不良事件的报告频率高于385例接受类似治疗方案的成人克罗恩病患者:贫血(10.7%)、便血(9.7%)、白细胞减少症(&7%)、潮红(8.7%)、病毒感染(7.8%)、中性粒细胞减少症(6.8%)、骨折(6.8%)、细菌性感染(5.8%)和呼吸道过敏反应(5.8%)。
REACH研究中有56.3%的随机分组受试者报告了感染,ACCENT1硏究中有50.3%接受本品5mg/kg的受试者报告了感染。在REACH研究中,每8周输液的受试者报告感染的频率高于每12周输液的受试者(分别为73.6%和38.0%),每8周维持治疗组和每12周维持治疗组分别有3例和4例受试者报告了严重感染。最常报告的感染为上呼吸道感染和咽炎,最常报告的严重感染为脓肿。有3例患者报告了肺炎,其中每8周维持治疗组有2例,每12周维持治疗组有1例。每8周维持治疗组有2例患者报告了带状疱疹。
总体而言,在REACH研究中,17.5%的随机分组患者发生了1次或多次的输液反应,在每8周和每12周维持治疗组中分别为17.0%和18.0%。REACH研究中没有严重输液反应,有2例受试者发生了非严重的速发过敏反应。
有3例(2.9%)儿童患者产生了本品的抗体。
老年患者(≥65岁)
类风湿关节炎的临床研究中,65岁及以上患者合用本品与甲氨蝶吟治疗比65岁以下患者的严重感染发病率高,分别为11.3%和4.6%。65岁及以上患者单用甲氨蝶吟治疗比65岁以下患者的严重感染发病率高,分别为5.2%和2.7%。
上市后用药经验
本品上市后,在成人和儿童患者中报告有不良反应。由于这些事件为自发性报告,且样本量不确定,因此,很难确定其发生率,也不能明确事件与使用本品的因果关系。
在本品上市后的使用过程中,报告了以下不良反应,某些甚至为死亡,具体包括:中性粒细胞减少(包括尚未出生但在子宫中暴露于本品的婴儿)、间质性肺病(包括肺纤维变性/间质性肺炎和快速进展性疾病)、特发性血小板减少性紫瘢、血栓性血小板减少性紫瘢、心包积液、全身和皮肤脉管炎、多形性红斑、史蒂文斯-约翰逊综合征、中毒性表皮坏死溶解、外周脱髓鞘病(如:格-巴二氏综合征、慢性炎性脱髓鞘性多发性神经病和多灶性运动性神经病变)、开始本品输注后大约24小时内发生的脑血管意外、新发的和加重的银屑病(包括脓疱样的所有亚型,主要见于掌跖)、横贯性脊髓炎和神经病变(也观察到了其它神经病学反应)、急性肝功能衰竭、黄疸、肝炎和胆汁郁积、严重感染、原虫感染、(在子宫中暴露于本品后)由疫苗注射爆发的感染(包括弥散性卡介苗感染的牛结核)和恶性肿瘤(包括黑色素瘤、宫颈癌和Merkel细胞癌)。
儿童用药的上市后经验中最常报告的严重不良事件为感染(有些致死),包括机会性感染和结核病、输液反应和超敏反应。本品用于儿童的上市后经验中,自发性严重不良事件也包括恶性肿瘤、一过性肝酶异常、狼疮样综合征和自身抗体阳性。
接受本品治疗的患者中曾报告过肝脾T细胞淋巴瘤的上市后病例,绝大多数病例发生于克罗恩病和溃疡性结肠炎,其中大部分为青少年或年轻成年男性。接受本品治疗的患者中罕有嗜血细胞性淋巴组织细胞增生症的报道。
输液相关性反应:
在上市后使用中,曾出现过敏反应病例,包括喉/咽部水肿、重度支气管痉挛以及癫痫。
在本品治疗中,输液期间或者输液后2小时内曾报告短暂性视力丧失病例以及开始输注后24小时内曾报告心肌缺血/梗死和心率不齐病例。
•对英夫利西单抗、其它鼠源蛋白或本品中任何成份过敏的患者。
•患有结核病或其它活动性感染(包括脓毒症、脓肿、机会性感染等)的患者。
•患有中重度心力衰竭(纽约心脏学会心功能分级III/IV级)的患者。
警示语:严重感染和恶性肿瘤
严重感染
使用本品进行治疗的患者发生严重感染的风险增高,可导致住院或死亡。发生感染的多数患者正在合并使用免疫抑制剂,如甲氨蝶吟或糖皮质激素。
如果患者发生严重感染或脓毒症,应停用本品。
报告的感染包括:
·活动性结核病,包括潜伏性结核病的复发。结核病患者经常伴随出现弥散性或肺外疾病。需在本品治疗前及治疗期间检测患者是否存在潜伏性结核病。如检查结果为阳性,则应在本品用药前对潜伏性结核病进行治疗。
·侵袭性真菌感染,包括:组织胞浆菌病、球施子菌病、念珠菌病、曲霉病、芽生菌病和肺囊虫病。组织胞浆菌病或其它侵袭性真菌感染患者多表现为弥散性,而非局灶性的疾病。在某些存在活动性感染的患者中,组织胞浆菌病的抗原和抗体检测结果可能是阴性的。若重度系统性疾病患者存在发生侵袭性真菌感染的危险,应考虑进行经验性的抗真菌治疗。
·细菌、病毒及其它条件致病菌导致的感染,包括军团杆菌和李斯特菌。
对慢性或复发性感染患者治疗前,应慎重考虑本品治疗的风险和获益。
在本品治疗期间及治疗后,应密切监测患者是否出现感染的症状和体征,包括开始治疗前潜伏性结核病感染检测结果为阴性的患者。
恶性肿瘤
有报告显示,儿童和青少年患者使用包括本品在内的肿瘤坏死因子(TNF)抑制剂治疗时,有淋巴瘤和其它恶性肿瘤的发生,其中有些是致命的。
本品上市后,已经有报告在接受包括本品在内的TNF抑制剂治疗的患者中出现了肝脾T-细胞淋巴瘤(HSTCL)病例,这是一种罕见的T-细胞淋巴瘤。这些病例的病程呈侵袭性,可以导致死亡,绝大多数发生在克罗恩病或溃疡性结肠炎患者中,且大多数为青少年或青年男性。几乎上述所有患者均在接受TNF抑制剂时或之前短时间内接受过硫唑嘌呤或6-巯基嘌呤的治疗。
严重感染
在接受本品治疗的患者中,发生严重感染的风险会增高,其中涉及了不同器官系统和部位,可能导致住院或死亡。
已经有报告在使用TNF抑制剂时,患者会出现因细菌、分枝杆菌、侵袭性真菌、病毒或寄生虫导致的机会性感染,包括曲霉病、芽生菌病、念珠菌病、球跑子菌病、组织胞浆菌病、军团杆菌、李斯特氏菌病、肺囊虫病和结核病。患者多表现为弥散性,而非局灶性的病变。
活动性感染的患者不应使用本品治疗,包括临床上重要的局部感染。对于年龄大于65岁,存在合并疾病和/或同时服用糖皮质激素或甲氨蝶吟等免疫抑制剂的患者,其发生感染的风险会增高。在以下患者中,应在本品治疗开始前考虑治疗的风险和收益:
•有慢性或复发性感染;
•接触过结核病患者;
•存在机会性感染病史;
•在结核病或霉菌病的流行地区居住或旅行过的,如组织胞浆菌病、球弛子菌病 或芽生菌病;
•罹患易于感染的病症。
结核病
在接受本品治疗的患者中,包括之前接受过潜伏性或活动性结核病治疗的患者中,已观察到活动性结核病病例,包括结核病复发或者新发结核感染。应注意报告的活动性结核病大多发生在肺外,有局灶性也有弥散性疾病。接受本品治疗的患者中,有在治疗潜伏性结核病期间发生活动性结核病的病例。
应在开始本品治疗前以及治疗期间定期评估患者是否存在结核病风险因素并检测是否存在活动或潜伏性感染。评估应包括患者的详细病史,包括结核病史、既往与结核患者密切接触史以及既往和当前接受免疫抑制治疗的情况。应对所有患者进行筛查,包括胸部影像学(推荐胸部CT)和结核菌素试验,有条件者建议行结核分枝杆菌抗原特异性T细胞酶联免疫斑点试验(Tcell enzyme-linked immune-spot assay.T-SPOT.TB)。如确诊有活动性结核,不可使用本品治疗。
如果怀疑有潜伏性结核病,应咨询有结核病治疗专业知识的医生。如确诊有潜伏性结核病,应于本品治疗前遵从当地建议采用抗结核疗法治疗潜伏性结核病。己有显示在接受TNF抑制剂治疗前对潜伏性结核感染进行治疗可以降低治疗期间结核病复发的风险。在评价是否需要于本品治疗前对患潜伏性结核病的患者进行治疗时,即使是之前接种过卡介苗(BCG)的患者,若结核菌素皮肤试验显示存在5mm或更大的硬结,应考虑检测结果属于阳性。需提醒处方医师,结核菌素皮试结果有假阴性风险,尤其是那些病重或免疫功能低下的患者更易得出假阴性结果。
对于既往有潜伏性或者活动性结核病史、但无法证实是否进行了足够疗程治疗的患者,以及潜伏性结核病检测结果为阴性、但存在结核感染危险因素的患者,应在开始本品用药前考虑接受抗结核治疗。在决定抗结核治疗是否适用于某一个体患者时,建议咨询在结核病治疗方面具有专业经验的医师。
对于本品治疗期间出现的新发感染,尤其是在之前或最近曾到过结核病高发国家旅行过的或者曾密切接触过患有活动性结核病患者的患者,强烈建议考虑结核病。应告知所有患者,如在本品治疗过程中或治疗后发生结核性体征/症状(即持续咳嗽、消瘦/体重下降、低热),则应寻求医疗救治。
监测
在接受本品治疗期间及治疗后,应密切监测患者是否出现感染的症状和体征,包括对开始治疗前潜伏性结核感染检测结果为阴性的患者。在本品治疗期间,潜伏性结核感染检测结果也可能呈假阴性。
在接受本品治疗期间,应定期评估结核风险,警惕肺外结核和播散性结核。治疗期间一旦诊断活动性结核,应立即停用本品,并予适当的抗结核治疗。
如果患者发生严重感染或脓毒症,应停用本品。对于本品治疗期间出现新发感染的患者,应采用一套适用于免疫缺陷患者的快捷、完整的诊断工序给予密切监测,同时应开始适当的抗菌治疗。
侵袭性真菌感染
对于在存在地方性霉菌病的地区居住或旅行过的患者,如果发生了严重的系统性疾病,应怀疑侵袭性真菌感染。应考虑在诊断期间对患者进行适当的经验性抗真菌治疗。某些存在活动性感染的患者中,组织胞浆菌病的抗原和抗体试验结果可能为阴性。如果可行,应咨询在侵袭性真菌感染诊断和治疗方面具有专业经验的医师来决定是否对该类患者进行抗真菌治疗,并考虑重度真菌感染与抗真菌治疗的风险。
恶性肿瘤
在接受包括本品在内的TNF抑制剂治疗的儿童、青少年和年轻成人中(治疗开始时的年龄勺8岁)已经报告出现过恶性肿瘤病例,有些致死。其中大约一半的病例为淋巴瘤,包括霍奇金和非霍奇金淋巴瘤。剩余的病例可表现为其它恶性肿瘤,包括通常与免疫抑制有关的、罕见的恶性肿瘤以及不常在儿童和青少年中观察到的恶性肿瘤。恶性肿瘤的中位发生时间是首剂TNF抑制剂治疗后的30个月(范围:1~84个月)。多数患者正在接受合并的免疫抑制剂治疗。这些病例多在药品上市后报告,来自多个国家,包括登记的和自发的上市后报告。
淋巴瘤
在所有TNF抑制剂临床试验的对照研究中,与对照组相比,在接受TNF抑制剂治疗的患者中观察到了较多的淋巴瘤病例。在本品临床试验的对照研究和开放性研究中,5707名接受本品治疗的患者中,有5名患者出现了淋巴瘤(中位随访持续时间是1.0年),而在1600名对照组患者中,无患者出现淋巴瘤(中位随访持续时间是0.4年)。在类风湿关节炎患者中,在每100患者-年的随访时间中观察到了2例淋巴瘤病例,发病率为0.08,与普通人群中预期的数值相比大约高出3倍。在汇总的类风湿关节炎、克罗恩病、银屑病关节炎、强直性脊柱炎、溃疡性结肠炎和斑块型银屑病临床试验人群中,在每100患者-年的随访时间中观察到了5例淋巴瘤病例,发病率为0.10,与普通人群中预期的数值相比大约高出4倍。克罗恩病、类风湿关节炎或斑块型银屑病患者,尤其是罹患高度活动性疾病和/或长期接受免疫抑制剂治疗的患者,即使是在无TNF抑制剂治疗时,其发生淋巴瘤的危险可能要高于普通人群(高达几倍)。在TNF抑制剂上市后应用于类风湿关节炎和其它适应症时,曾报告过急性和慢性白血病病例。即使是在无TNF抑制剂治疗的情况下,类风湿关节炎患者发生白血病的危险也可能要高于普通人群(大约2倍)。
儿童恶性肿瘤
接受TNF抑制剂(治疗开始时白8岁)(包括本品)用于治疗青少年特发性关节炎(JIA)、克罗恩病或其他病况的儿童、青少年和年轻成人(最大至22岁)患者中曾报告过上市后的恶性肿瘤病例,其中一些导致死亡。大约一半的报告为淋巴瘤。其他病例涉及多种不同的恶性肿瘤,包括不常见于儿童和青少年的恶性肿瘤。大部分患者合并使用免疫抑制剂,例如甲氨蝶吟、硫唑嘌呤或6-巯嘌呤。TNF抑制剂在儿童和青少年恶性肿瘤发生过程中发挥的作用仍然不明。
肝脾T-细胞淋巴瘤(HSTCL)
本品上市后,已经有报告在接受包括本品在内的TNF抑制剂治疗的患者中出现了肝脾T-细胞淋巴瘤(HSTCL)病例,这是一种罕见的T-细胞淋巴瘤。这些病例的病程呈侵袭性,可以导致死亡,绝大多数发生在克罗恩病或溃疡性结肠炎患者中,且大多数为青少年或青年男性。几乎上述所有患者均在接受TNF抑制剂时或之前短时间内接受过硫唑嘌呤或6-巯基嘌呤的治疗。目前尚不确定HSTCL的发生是否与TNF抑制剂或TNF抑制剂与上述其它免疫抑制剂的联用有关。在对炎性肠病患者进行治疗时,特别是在青少年和年轻成人中,基于临床试验数据中获得的本品单药治疗时观察到的免疫原性与过敏反应增高的风险,以及联合治疗可能导致HSTCL的发生危险增高,应考虑选择本品单用还是与其它免疫抑制剂联用。当考虑给予患者英夫利西单抗单药治疗还是与其他免疫抑制剂如硫哩嗦吟或6-筑基喋吟联合治疗时,根据临床试验数据,需要权衡以下可能性,即联合治疗的HSTCL风险更高,反之观察到英夫利西单抗单药治疗的免疫原性和超敏反应风险增加。
皮肤癌
在己经使用TNF抑制剂治疗包括使用本品的患者中已有黑色素瘤和Merkel细胞癌的报告。建议病人做定期的皮肤检查,特别是皮肤癌风险高的患者。
宫颈癌
一项基于人群的回顾性队列研究发现,与未接受过生物制剂组或普通人群(包括60岁以上)相比,使用英夫利西单抗的类风湿性关节炎女性患者中宫颈癌的发生率升高。不排除本品与宫颈癌的因果关系。包括60岁以上的女性患者使用本品需进行定期筛查。
其它恶性肿瘤
在包括本品在内的某些TNF抑制剂临床试验的对照部分,与对照组患者相比,在接受TNF抑制剂治疗的患者中观察到了较多的恶性肿瘤病例[不包括淋巴瘤和非黑色素瘤皮肤癌(NMSC)]。在中重度类风湿关节炎、克罗恩病、银屑病关节炎、强直性脊柱炎、溃疡性结肠炎和斑块型银屑病患者中进行的本品试验的对照部分,4019名接受本品治疗的患者中,有14名患者被确诊为恶性肿瘤(不包括淋巴瘤和NMSC),而在1597名对照组患者中,只有1名患者出现恶性肿瘤(本品治疗组患者的发生率为0.52/100患者-年,对照组患者的发生率为0.11/100患者-年),本品治疗组患者的中位随访持续时间是0.5年,对照组为0.4年。其中,最常见的恶性肿瘤是乳腺癌、结肠直肠癌和黑色素瘤。本品治疗组患者中恶性肿瘤的发生率与普通人群中预期的发生率近似,而对照组患者低于普通人群的预期发生率。
在中重度慢性阻塞性肺病(COPD)临床试验中,与对照组患者相比,本品治疗组患者报告了更多的恶性肿瘤病例,其中大多数为肺部或头颈部。所有的患者均存在重度吸烟史。在中重度COPD患者中使用本品时,处方医师应谨慎用药。
应监测银屑病患者是否出现非黑色素瘤皮肤癌(NMSCs),特别是那些既往接受过长期光照治疗的患者。在本品临床试验的维持治疗部分,显示NMSCs更常见于之前进行过光照治疗的患者。
TNF抑制剂治疗在恶性肿瘤发生中可能起到的作用尚不清楚。本品临床试验中所显示的疾病发生率无法与其它TNF抑制剂临床试验中的发生率相比较,也不可以用于预测更广泛患者群中观察到的发生率。在考虑对存在恶性肿瘤病史的患者进行本品治疗,或者是考虑对本品治疗期间发生了恶性肿瘤的患者继续治疗时,应慎重。
结肠不典型增生或结肠癌风险增加(例如长期溃疡性结肠炎或原发性硬化性胆管炎患者)或有不典型增生或结肠癌病史的所有溃疡性结肠炎患者,应在治疗前和整个病程中定期筛查不典型增生。按照当地建议,此评价应包括结肠镜和活组织检查。现有数据未明确本品治疗是否会影响发生不典型增生或结肠癌的风险。由于接受本品治疗的新发不典型增生的患者发生癌症风险增加的可能性尚未建立,因此应谨慎评价患者个体的风险和获益,并应考虑停药。
乙型肝炎病毒再激活
在慢性病毒携带者(如表面抗原阳性)中,使用包括本品在内的TNF抑制剂,曾出现过乙型肝炎病毒(HBV)再激活的病例。某些情况下,伴随TNF抑制剂治疗出现的HBV再激活可能是致死性的。其中大多数的报告发生在同时接受其它系统性免疫抑制药物治疗的患者中,这些药物也会导致HBV再激活。
在开始包括本品在内的TNF抑制剂治疗前,应根据国内现行指南检测患者是否出现HBV感染。对于乙型肝炎表面抗原检测结果呈阳性的患者,建议咨询在乙型肝炎治疗方面具有专业经验的医师,预防性使用适当的药物抗病毒治疗。对于HBV携带者,联合抗病毒治疗与TNF抑制剂治疗的安全性或疗效尚未获得充足的数据。对于需要接受TNF抑制剂治疗的HBV携带者,在整个治疗期间应密切监测是否出现活动性HBV感染的临床和实验室指征,并在治疗结束后的几个月继续进行监测。在发生HBV再激活的患者中,应停用TNF抑制剂,并开始抗病毒治疗以及适当的支持治疗。目前尚不清楚HBV再激活后重新开始TNF抑制剂治疗的安全性。因此,此种情况下处方医师应谨慎考虑恢复TNF抑制剂的治疗并给与患者密切监测。
肝脏毒性
在接受本品治疗的患者中,上市后数据中已有报告重度肝脏反应,包括急性肝功能衰竭、黄疸、肝炎和胆汁淤积,其中某些病例被确诊为自身免疫性肝炎。一些肝脏反应发生于本品开始治疗后的2周至超过一年,其中的许多病例在发现肝脏损伤前并未观察到肝转氨酶水平的增高,某些病例是致死性的或必须进行肝脏移植。对于出现肝功能不全症状或体征的患者,应评估是否存在肝损伤的证据。如果出现黄疸和/或显著的肝酶增高(例如,大于5倍的正常范围上限),应停用本品,并对异常进行全面的检查。在临床试验中,已经在接受本品治疗的患者中观察到了轻度或中度的ALT和AST增高,但没有进展至重度肝损伤的病例。
心力衰竭患者
在心力衰竭患者中,本品治疗会伴随出现不良结果,只在其它治疗不可行时才可在心力衰竭患者中使用本品。在评价心力衰竭(NYHA心功能分级为III/IV级)患者使用本品的随机分组研究中,接受10mg/kg本品治疗的患者死亡率增髙,5mg/kg和10mg/kg剂量组心血管不良事件的发生率增高。已有过本品用药患者出现心力衰竭加重的上市后报告(存在或不存在可鉴别的预测因素)。新发心力衰竭上市后罕有报告,包括对既有心血管疾病不知情的患者,其中某些患者年龄小于50岁。如果决定对心力衰竭患者使用本品,则应在治疗期间给予密切监测,且在出现新的心力衰竭症状或症状加重时停用本品。
输液反应/过敏反应
本品治疗可能伴随出现过敏反应(包括过敏性休克和迟发性超敏反应),但发生时间较为多变,某些病例可能需要住院。多数过敏反应(包括尊麻疹、呼吸困难和/或支气管痉挛、喉水肿、咽部水肿和低血压)发生于本品输注期间或者输注后2小时内。
不过,在某些病例中,于最初的英夫利西单抗治疗后(即早在第二剂后),以及在长时间本品治疗停止后重新开始本品治疗时,在患者中观察到了血清病样反应。伴随上述反应会出现以下症状:发热、皮疹、头痛、咽喉痛、肌痛、多关节痛、手面部水肿和/或吞咽困难。这些反应会伴随出现显著的英夫利西单抗抗体增高、无法检测到英夫利西单抗的血清浓度以及可能丧失药物疗效。
若出现重度过敏反应,应停用本品。医院需配备治疗过敏反应的药物(例如,对乙酰氨基酚、抗组胺药、糖皮质激素和/或肾上腺素)。
在类风湿关节炎、克罗恩病和银屑病临床试验中,与规律的维持治疗相比,经过一个阶段停药后,重新给予本品会使输液反应的发生率增高。经过一段时间停药后重新给予本品,特别是决定重新开始0、2和6周诱导方案时,应认真考虑收益-风险比。如银屑病患者维持治疗中断,不推荐再次启动诱导治疗,应按照维持治疗再次给药。
自身免疫
使用本品治疗可能会促使自身抗体的形成以及狼疮样综合征的出现。若患者在接受本品治疗时出现狼疮样综合征征兆,则应立即停药。
神经系统
本品和其它TNF抑制剂的用药中会伴随出现系统性脉管炎、癫痫、中枢神经系统性脱髓鞘病新发临床症状或原有症状加重和/或出现放射学证据(包括多发性硬化、视神经炎)以及外周性脱髓鞘病(包括格林-巴利综合征)。处方医师应慎重考虑在出现上述神经学异常的患者中使用本品,并应在发生该类异常时停用本品。
与阿那白滞素合用
在阿那白滞素与TNFa抑制剂依那西普合用的临床试验中,曾观察到严重感染及中性粒细胞减少症的病例,与单独使用依那西普相比,联合用药并未增加疗效。根据阿那白滞素与依那西普合用发现的不良反应的性质,可推测出阿那白滞素与其它TNFa抑制剂合用可能产生类似的不良反应。因此,不建议本品与阿那白滞素合并使用。
与阿巴西普合用
在临床试验中,TNFa抑制剂与阿巴西普合用与单独使用TNFa抑制剂相比,其感染(包括严重感染)的风险增加,而疗效并未加强。因此,不建议本品与阿巴西普合用。
与其它生物制剂疗法合用
尚无本品与其相同适应症的其它生物制剂合用的充分信息。不建议本品与其具有相同适应症的生物制剂合用,因合用可能增加感染风险。
与生物制剂疗法间的转换
应慎重从一种生物制剂转换为另一种,因为生物活性叠加可进一步增加感染的风险。
如果更换生物制剂,需要继续对患者进行感染的监测。
对血液系统的影响
在接受本品治疗的患者中,己经有白细胞减少、中性粒细胞减少、血小板减少症和全血细胞减少症的病例报告,某些可致死。但事件与本品治疗的因果关系仍不明确。虽然尚未确立高危人群,但对于正在患有或者有过显著血液学异常病史的患者,在接受本品治疗时应慎重。建议所有的患者若在本品治疗期间出现提示血恶液质或感染的症状或体征(例如,持续发热)时,应立即寻求医疗救治。如果患者出现显著的血液学异常,应考虑停止本品治疗。
疫苗接种/治疗用感染性制剂
在接受TNF抑制剂治疗的患者中,有关活疫苗接种后的反应或者活疫苗接种后继发性感染传播的数据有限。活疫苗接种可能引起包括弥散性感染在内的临床感染。建议患者不要同时接种活疫苗。妊娠期间接受过本品治疗的女性患者的婴儿在接种活疫苗时应慎重,因为本品可通过胎盘,已经于妊娠期间接受过本品治疗的女性患者的婴儿血清中检测到过本品,持续时间最长可达6个月。
报告一例在子宫中暴露于英夫利西单抗的婴儿出生后接受卡介苗导致弥散性卡介苗感染而死亡。建议婴儿如在子宫中暴露于英夫利西单抗,在出生后至少6个月后方可接受活疫苗。
治疗用感染性制剂的其他应用,如减毒活细菌(例如,治疗肿瘤的膀胱内灌注的卡介苗)的使用也可能引起包括弥散性感染在内的临床感染。建议不要将治疗用感染性制剂与本品同时使用。建议所有患者在开始英夫利西单抗治疗之前,接种现阶段所需的所有疫苗。接种疫苗与开始英夫利西单抗治疗之间的间隔应按照目前的疫苗接种指南。
其它
接受本品治疗又接受外科手术(包括关节成形术)的患者的安全性资料有限。如计划实施外科手术,应考虑到英夫利西单抗的半衰期较长的因素。在外科手术后应密切监测使用本品治疗患者的感染情况,并釆取适当措施。
克罗恩病治疗无效可能表明患者有顽固的纤维化狭窄,可能需要手术治疗。未有证据显示英夫利西单抗会使其恶化或引发纤维化狭窄。
本品与其未被认为可互换的生物类似药的转换或替代使用的安全性和有效性尚未确立。因此不建议本品与其生物类似药之间的转换或替代使用。
与阿那白滞素或阿巴西普联用
在其它TNFa抑制剂与阿那白滞素或阿巴西普联用的临床试验中,观察到发生严重感染的风险增高,但未显示临床获益增加。鉴于TNFa抑制剂联合治疗中所观察到的不良反应的发生机理,联合使用阿那白滞素或阿巴西普和其它TNFa抑制剂可能会导致类似的毒性。因此,不建议本品和阿那白滞素或阿巴西普联合使用。
与托珠单抗联用
托珠单抗与生物性改善病情抗风湿药(DMARDs)(如TNF抑制剂,包括本品)联合使用,潜在发生免疫抑制的可能和感染的风险会增高。应避免托珠单抗与本品合用。
与其它生物制剂联用
不建议本品与其具有相同适应症的其它生物制剂合用。
甲氨蝶吟(MTX)和其它合并用药
尚未进行特定的药物(包括MTX)相互作用研究。在类风湿关节炎或克罗恩病临床试验中,大多数的患者接受了一种或者多种合并用药。在类风湿关节炎研究中,除MTX外的合并用药包括:非釦本类抗炎药(NSAIDs)、叶酸、糖皮质激素和/或麻醉药。克罗恩病研究的合并用药包括:抗生素、抗病毒药、糖皮质激素、6-MP/AZA和氨基水杨酸盐。在银屑病关节炎临床试验中,合并用药包括:MTX(大约一半的患者)、NSAIDs、叶酸和糖皮质激素。合并使用MTX可能会减少抗英夫利西单抗抗体的产生,使英夫利西单抗浓度升高。
免疫抑制剂
与不接受免疫抑制剂的患者相比,接受免疫抑制剂治疗的克罗恩病患者有出现较少输液反应的趋势。基线时使用克罗恩病治疗药物没有出现对英夫利西单抗血清浓度明显的影响,涉及的药物包括:糖皮质激素、抗生素(甲硝哩或环丙沙星)和氨基水杨酸盐。
细胞色素P450底物(CYP450)
慢性炎症时,CYP450酶的形成可能会因细胞因子水平[例如,TNFa、白介素-1(IL-1)、白介素-6(IL-6)、白介素-10(IL-10)和干扰素(IFN)]的增高而受到抑制。因此,能够拮抗细胞因子活性的分子(如英夫利西单抗)预计可以使CYP450酶的形成趋于正常。若在接受治疗指数狭窄的CYP450底物药物治疗的患者中开始或停用本品,建议监测这类药品的疗效(例如,华法林)或药物浓度(例如,环砲霉素或茶碱),并根据需要调整此类药品的剂量。
活疫苗/治疗用感染性制剂
建议使用本品的患者不要同时接种活疫苗或使用治疗用感染性制剂。
同时也建议宫内暴露于英夫利西单抗的婴儿在出生后至少6个月后再接种活疫苗。
【药物过量】
单次给药剂量达到20mg/kg时未出现直接的毒性反应。当过量给药时,建议监测患者不良反应或有效性的任何症状或体征,并及时采取恰当的对症治疗。
【临床试验】
类风湿关节炎
经ATTRACT(合并用药治疗类风湿关节炎的抗TNF试验)和ASPIRE(使用本品治疗类风湿关节炎早期发作的活性对照试验)两个多中心、随机、双盲临床试验,对本品的安全性和有效性进行了评价。在试验中可以合并使用稳定剂量的叶酸、糖皮质激素口服制剂(MlOmg/日)和/或非階体抗炎药。终点的主要指标为根据美国风湿病学会(ACR)标准评定症状和体征的减轻、预防关节结构损害和改善身体机能。
在428名活动性类风湿关节炎患者(合用甲氨蝶吟)参加的安慰剂对照ATTRACT试验中,对第30>54和102周时的疗效进行了评价。入组患者的年龄中位值为54岁,患病期中位值为8.4年,肿胀关节数和触痛关节数中位值分别为20和31。约50%患者的身体机能为III级。患者被分为安慰剂组、3mg/kg英夫利西单抗组或lOmg/kg英夫利西单抗组,分别于第0、2和6周给药,随后每隔4周或8周给药。全部患者在入组前均使用6个月稳定剂量的甲氨蝶玲(剂量中位值为15mg/周),并在试验过程中维持该稳定剂量。
ASPIRE试验评价了1004名未用甲氨蝶玲的早期(患病期v3年)活动性类风湿关节炎患者在第54周的疗效。入组患者年龄中位值为51岁,患病期中位值为0.6年,肿胀关节数和触痛关节数中位值分别为19和31。全部患者在第0、2和6周以及以后每8周时接受安慰剂、3mg/kg本品或6mg/kg本品,同时合用甲氨蝶吟(在第8周前将剂量优化至20mg/周).在上述试验中,前3次的输注时间应超过2小时,未出现严重输液反应的患者可以将之后的输注时间缩短,但不得少于40分钟。
临床疗效
症状和体征的减轻定义为在关节肿痛方面和以下5个标准中的3个都有至少20%的改善,即ACR20o这5个标准是:医师总体评定、患者总体评定、功能/残疾评估、视觉模拟疼痛量表、红细胞沉降率(ESR)或C-反应蛋白(CRP)。
在ATTRACT试验中,合用甲氨蝶吟的本品全部剂量及疗程组在54周中对症状和体征的改善均达到了美国风湿病学会标准的ACR20(图1)。对症状和体征具有统计学意义的改善(ACR20)可持续至第102周。
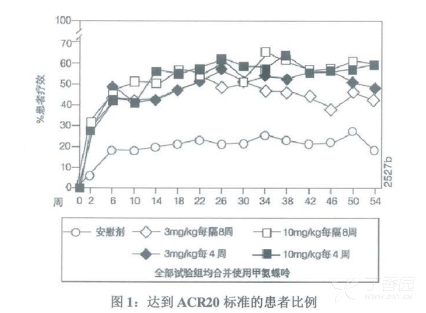
在ATTRACT试验中,英夫利西单抗组中达到ACR50和ACR70的患者多于安慰剂组(表3)。在获得显著疗效(定义为6个月维持ACR70的效果)的患者比例上,英夫利西单抗组约为10%,而安慰剂组为0%(p<0.018)。
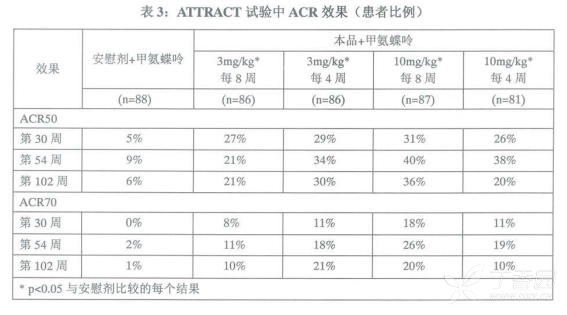
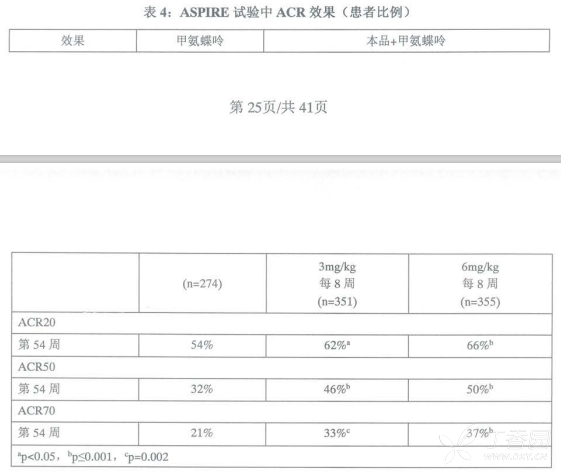
在ASPIRE试验中,治疗54周后,在改善患者症状体征达到ACR20、ACR50和ACR70的比例上,本品各剂量组均显著高于甲氨蝶吟单独用药组(表4)。在获得显著疗效的患者比例上,英夫利西单抗组为15%,而甲氨蝶吟单独用药组为8%(p=0.003)。
放射学检查显示的疗效
在第54周,通过放射学检查对手部和足部的关节结构损害(侵蚀及关节腔狭窄)进行van der Heijde-modified Sharp评分,该评分是对手/腕部和足部关节侵蚀数量和程度以及关节腔狭窄程度等结构损害进行评价的一种合成分数。
在ATTRACT试验中,约80%患者有放射学对照资料,结果列于表5。在第54周获得的具有统计学意义的防止关节损害发展的疗效可持续至第102周。

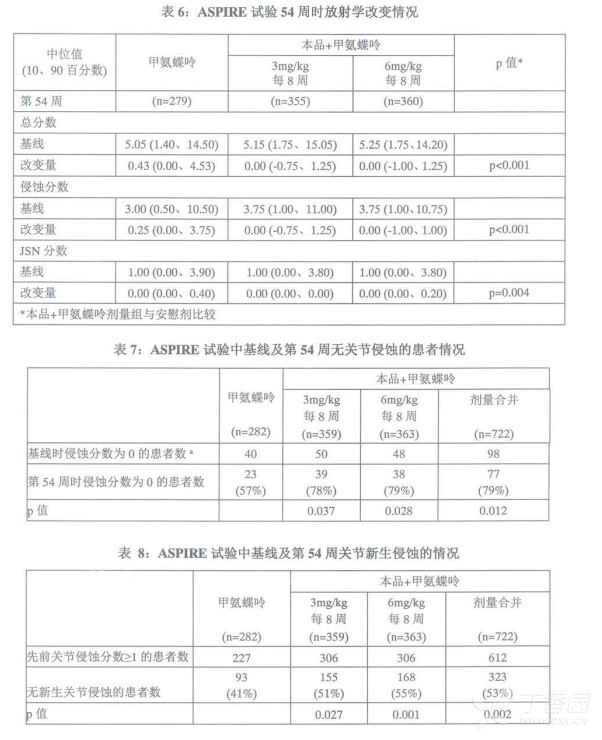
在ASPIRE试验中,90%以上患者有至少2个可评价的放射学影像资料。在第30和54周(表6),可观察到本品+甲氨蝶吟合用组和甲氨蝶吟单用组对关节损害发展的抑制效果分别为97%和86%。在维持关节免于侵蚀的效果上(表7),本品+甲氨蝶吟合用组(79%)明显优于甲氨蝶吟单用组(57%)。在关节新生侵蚀的患者比例上(表8),本品+甲氨蝶吟合用组(47%)明显少于甲氨蝶吟单用组(59%)。
身体机能的改善
在ATTRACT试验的102周中,在改善身体机能方面,本品+甲氨蝶吟的各剂量/疗程组的效果明显优于安慰剂+甲氨蝶吟组。经简明健康调查问卷(SF-36)对与健康相关的生活质量进行了评价。SF-36的8个次级评定并入2个总评分(身体总评分和精神总评分)。在102周中,本品+甲氨蝶吟的各剂量/疗程组与安慰剂+甲氨蝶吟组相比,显示了对身体总评分的明显改善,同时未对精神总评分产生不良影响(表9)。

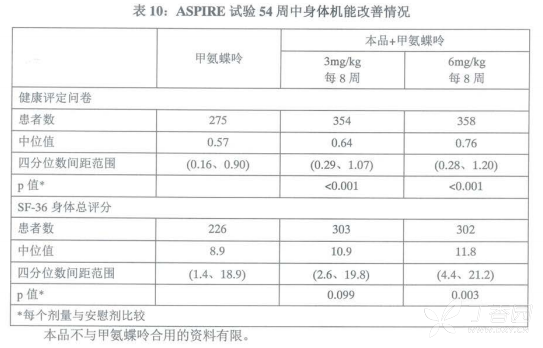
在ASPIRE试验的54周中,对于根据健康评定问卷评价的身体机能改善方面(表10),本品全部治疗组(0.7)的疗效显著优于甲氨蝶吟组(0.6),此差异具有统计学意义(p<0.001),同时未对SF-36精神总评分产生不良影响。
活动性克罗恩病
通过2项随机、双盲、安慰剂对照临床研究在653名对传统治疗无充分应答的中度至重度活动性克罗恩病患者[克罗恩病活动指数(CDAI)≥220,≤400]中评价了本品单剂量和多剂量的安全性和疗效。试验中允许伴随使用稳定剂量的氨基水杨酸盐、糖皮质激素和/或免疫调节制剂,92%的患者继续接受这些治疗中的至少1种药物。
在一项108名患者中进行的单剂量临床试验中,16%(4/25)的安慰剂组患者在第4周出现临床应答(CDAI降低Z70),而5mg/kg本品组为81%(22/27)(P<0.001,双侧检验,Fisher精确检验法)。另外,4%(1/25)的安慰剂组患者以及48%(13/27)的5mg/kg本品组患者在第4周达到临床缓解(CDAI<150)。
克罗恩病研究I(ACCENT I)多剂量临床试验中,545名患者在第0周接受一次5mg/kg本品,第2周出现临床应答的患者随机分至以下三个治疗组:安慰剂维持组在第2周、第6周及随后每8周给予安慰剂;5mg/kg维持组在第2周、第6周及随后每8周给予5mg/kg本品;10mg/kg维持组在第2周和第6周给予5mg/kg本品,随后每8周给予lOmg/kg本品。对第2周出现临床应答的患者与未出现应答的患者分别进行随机分组,第6周后允许糖皮质激素减量。
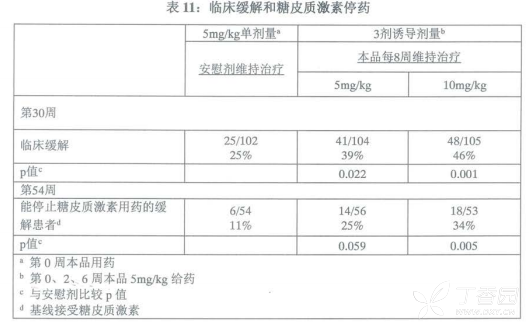
第2周时,57%(311/545)的患者达到临床应答。第30周时,与安慰剂维持组相比,5mg/kg和10mg/kg维持组出现临床缓解的患者显著增多(表11)。
此外,在第54周,与安慰剂维持组相比,本品5mg/kg及10mg/kg维持组出现临床缓解且可停止使用糖皮质激素的患者比例更大(表11)。
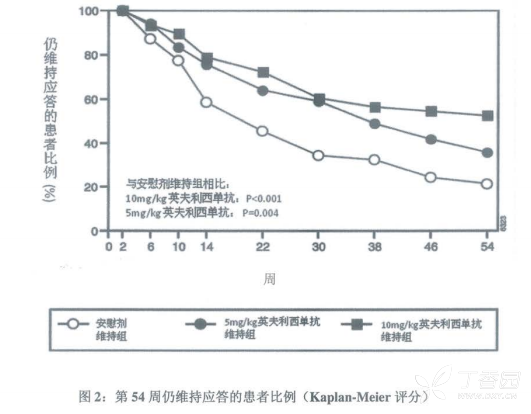
本品维持组(5mg/kg和10mg/kg)患者与安慰剂维持组相比,应答维持时间更长(图2)。
在第30周和第54周,5mg/kg和10mg/kg本品维持组与安慰剂维持组相比,疾病特异性炎性肠病调查问卷(IBDQ)评分较基线明显改善,尤其是在肠道方面和系统改善方面更加明显,而且SF-36中身体总评分也显著改善。
在基线岀现黏膜溃疡且参与内窥镜研究的78名患者中,第10周时,本品维持组13/43名患者内窥镜检査显示黏膜愈合,而安慰剂组1/28名患者达到黏膜愈合。第10周出现黏膜愈合的本品治疗患者中,9/12名患者在第54周也达到黏膜愈合。
获得应答但随后失去应答的患者将可接受比原随机分配剂量高出5mg/kg的本品治疗。这些患者多数能对较高剂量产生应答。在第2周未出现应答的患者中,59%(92/157)本品维持组患者在第14周出现应答,51%(39/77)安慰剂维持组患者出现应答。对于第14周未出现应答的患者,进一步治疗并未带来显著的临床应答。
瘘管性克罗恩病
通过2项在瘘管性克罗恩病成年患者(出现瘘管至少3个月)中进行的随机、双盲、安慰剂对照试验评价了本品的安全性和有效性。在研究中,允许患者同时使用糖皮质激素、5-氨基水杨酸、抗生素、甲氨蝶吟、6-巯嘌呤和/或硫唑嘌呤。
在第1项试验中,有94名患者在第0、2和6周接受安慰剂或本品治疗。此项临床试验中观察到5mg/kg本品组(p=0.002)和10mg/kg本品组(p=0.021)瘘管应答(在未增加药物或手术治疗的情况下,在连续至少2次随访中,克罗恩病患者轻压有引流液的肠外瘘数量降低250%)的患者比例分别为68%(21/31)和56%(18/32),而安慰剂组为26%(8/31)。本品组患者显效时间中位值和疗效持续时间中位值分别为2周和12周。本品组瘘管全部愈合的患者比例为52%,而安慰剂组的比例为13%(P<0.001)。
在第2项试验(ACCENTII)中,入组的患者至少有一个引流性肠外瘘(肛周、腹部)。所有患者在第0、2和6周接受5mg/kg本品治疗。患者第14周随机分配至安慰剂或5mg/kg本品维持组。患者在第14周接受维持剂量治疗,随后每8周进行一次治疗,直到第46周。第10周和14周均获得瘘管应答(瘘管应答定义与第1项试验中相同)的患者与失去应答的患者分开进行随机。试验的终点为从随机分组直至应答消失的时间。
在所有随机分组的患者(从296名中初步纳入273名患者)中,87%有肛周瘘,14%有腹瘘,8%有直肠阴道瘘。高于90%的患者曾使用过免疫抑制剂或抗生素。
第14周时,65%(177/273)的患者出现瘘管应答。本品维持组的应答持续时间长于安慰剂维持组(图3)。第54周时,本品组无引流性瘘管的患者比例为38%(33/87),安慰剂组为22%(20/90)(P=0.002)。与安慰剂维持组相比,本品维持组患者存在住院次数减少的趋势。

获得应答但随后失去应答的患者将可接受比原随机分配剂量高出5mg/kg的本品治疗。安慰剂维持组患者给予5mg/kg本品后,66%(25/38)出现应答,57%(12/21)的本品维持组患者对10mg/kg剂量出现应答。
对于第14周未出现应答的患者,进一步治疗并未带来显著的临床应答。
各组出现新瘘管的患者比例相似(总体上达17%),出现脓肿的患者数量相似(总体上达15%)。
儿童活动性克罗恩病
一项随机、开放性临床试验(REACH研究)在112例6〜17岁对传统治疗应答不足的中重度克罗恩病患者(儿童CDAI中值为40)中评价了本品的有效性和安全性。所有患者均需要接受稳定剂量的6-MP、AZA或MTX治疗(35%的患者在基线时也接受糖皮质激素治疗)。第0、2和6周给予5mg/kg英夫利西单抗治疗。第10周有临床应答的患者随机分配接受每8周或每12周5mg/kg英夫利西单抗维持治疗。允许维持治疗中失应答的患者转入高剂量(10mg/kg)组和/或缩短给药间隔(间隔8周)。第10周有临床应答的患者百分比为88.4%(99/112)。第10周有临床缓解的患者百分比为58.9%(66/112)。30周时给药间隔为8周组的临床缓解率较高(59.6%,31/52),给药间隔12周组较低(35.3%,18/51;p=0.013)。54周时,间隔8周维持治疗组和间隔12周维持治疗组数据分别为55.8%(29/52)和23.5%(12/51),p<0.001。
基线时接受糖皮质激素治疗的患者中,第30周时每8周维持治疗组患者无糖皮质激素临床缓解的比例为45.8%,而每12周维持治疗组为33.3%。第54周时每8周维持治疗组患者无糖皮质激素临床缓解的比例为45.8%,而每12周维持治疗组为16.7%。
强直性脊柱炎
一项对279例活动性强直性脊柱炎患者进行的随机、多中心、双盲、安慰剂对照研究评价了本品的安全性和有效性。患者(年龄为18~74岁)入组标准符合修订版纽约标准对强直性脊柱炎的定义。疾病处于活动期,Bath强直性脊柱炎活动性指数(BASDAI)评分>4且脊柱痛>4[视觉模拟评分(VAS)为0~10]。研究排除了脊柱完全强直的患者,并且禁止使用改善病情抗风湿药(DMARDs)和全身用糖皮质激素。患者分别在第0、2、6、12和18周通过静脉给予剂量为5mg/kg的本品或安慰剂。
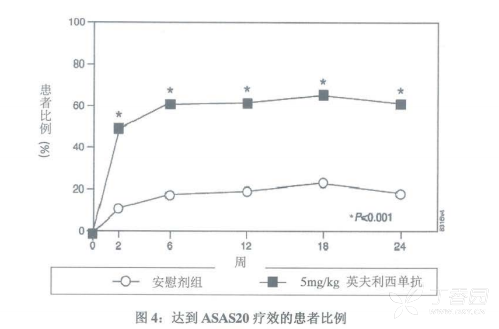
强直性脊柱炎症状和体征的改善情况通过ASAS(强直性脊柱炎评估)20疗效标准进行评价,在第24周,本品组和安慰剂组症状和体征改善达ASAS20疗效的患者比例分别为60%和18%(p<0.001)。此改善可在第2周被观察到,并且持续至第24周(图4和表12)。
在第24周,本品组达到ASAS50和ASAS70疗效的患者比例分别为44%和28%,而安慰剂组分别为9%和4%(P<0.001)。22%的本品组患者可达到低疾病活动状态[4个ASAS评估指标均<20(分数范围是0-100mm)],而安慰剂组仅为1%(P<0.001)。
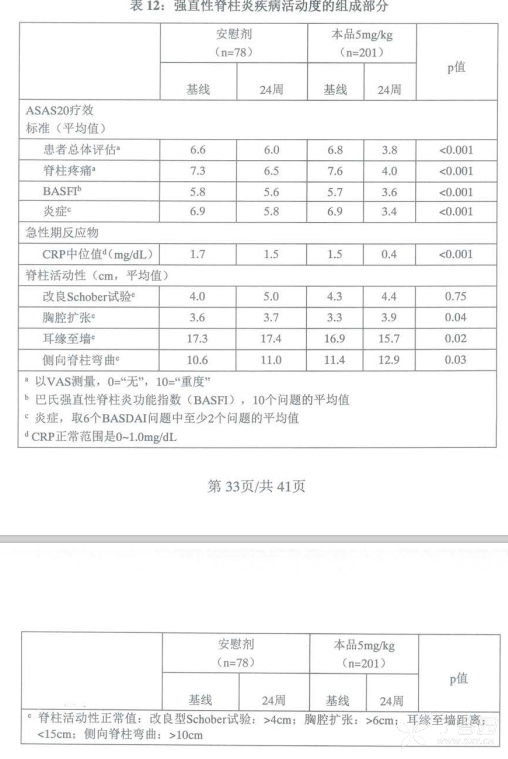
与健康相关的生活质量经SF-36进行评价,与基线相比,第24周时本品组SF-36躯体功能总体评分改善的中位值为10.2,而安慰剂组为0.8(P<0.001)。SF-36心理健康评分,本品组或安慰剂组均未发生变化。
此研究结果与一项70例强直性脊柱炎患者进行的多中心、双盲、安慰剂对照研究的结果相似。
斑块型银屑病
在评估英夫利西单抗安全性和有效性的3项随机、双盲、安慰剂对照研究中,受试者为18岁及18岁以上的慢性、稳定性斑块型银屑病患者,其体表面积(BSA)210%且银屑病面积和严重程度指数评分(PASD>12,适合系统治疗或光疗。点滴状、红皮病型或脓疱型银屑病患者被排除。研究期间不允许患者接受其它银屑病治疗,但在研究开始10周之后可以在面部和腹股沟处使用弱效外用糖皮质激素。
研究I(EXPRESS)在378例适合接受光疗或系统治疗的斑块型银屑病患者中评价了英夫利西单抗的诱导和维持疗法的有效性和安全性。患者在第0、2和6周输注5mg/kg英夫利西单抗或安慰剂,随后每8周接受一次维持治疗(安慰剂组至第22周;英夫利西单抗组至第46周)。在第24周时,安慰剂组患者交叉接受英夫利西单抗诱导治疗(5mg/kg),然后每8周接受一次维持治疗。在46周内,最初被随机分配为接受本品治疗的患者继续每隔8周使用剂量为5mg/kg的英夫利西单抗。所有治疗组的基线PASI评分中位值为21,基线的静态医生整体评估(sPGA)为中度(52%的患者)、显著(36%的患者)、重度(2%的患者)。此外,75%患者的BSA>20%。71%患者过去接受过系统治疗,82%接受过光疗。
研究II(EXPRESS II)评估了835例接受安慰剂或3mg/kg和5mg/kg剂量英夫利西单抗患者的有效性和安全性。在第0、2、6周的诱导期对他们进行评估。第14周时,将每个英夫利西单抗给药组的患者随机分为接受维持治疗的给药组(每8周给药一次)和按需要治疗的给药组(PRN),治疗持续到46周。第16周时,安慰剂组交叉至英夫利西单抗诱导治疗组(5mg/kg),之后进入到每8周的维持治疗(5mg/kg)»在所有治疗组中,基线PASI评分中位值为18,63%患者的BSA>20%。55%的患者过去接受过系统治疗,64%的患者曾接受过光疗。
研究III(SPIRIT)评价了249例曾经接受过补骨脂素联合紫外线照射(PUVA)或其它系统治疗的银屑病患者。这些患者在第0、2、6周随机接受安慰剂或者剂量为3mg/kg或5mg/kg的英夫利西单抗治疗。在26周时,sPGA评分为中度或显著的患者(得分不低于3分,分数范围是0~5分)接受随机剂量的一次额外治疗。在所有治疗组中,基线PASI评分的中位值为19,基线sPGA的评分是中度(62%患者)、显著(22%)、严重(3%)。此外,75%患者的BSA>20%。入组研究的患者中有114人(46%)在26周时使用了额外剂量的药物。
在研究I、II和III中,在第10周时主要终点为达到PASI75(PASI评分自基线改善75%)的患者比例。在研究I和研究HI中,另一种评价结果用sPGA评估包括达到清除或最轻患者的比例。sPGA是一种包含6个类别,评分范围从5=严重至0=清除来表示医生根据厚度、红斑和鳞屑来评估银屑病严重程度。治疗成功被定义为清除或最轻,包括无斑块突起或斑块突起很轻,皮疹呈淡红色,<5%的斑块上无或覆盖细小鳞屑。
研究II还根据相对性医生整体评估(rPGA)标准评估了达到清除或最小的患者百分比。rPGA以基线水平为基础,它包含6个类别,评分范围从6=严重至1=清除。总体病变的分级依据是皮疹面积占全身体表面积的百分比,以及厚度、鳞屑和红斑的程度。治疗成功被定义为清除或最轻,好转的标志是表现为粉红色或色素沉着的显著改善(接近正常的皮肤纹理;可能存在某些红斑),这些研究的结果如表13所示。
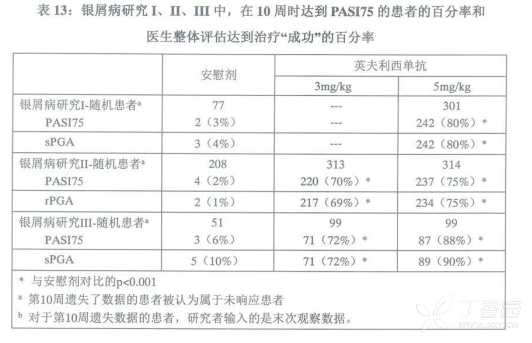
研究I里,对于银屑病皮疹面积更广泛且接受过光疗的患者亚组,使用5mg/kg英夫利西单抗的患者有85%在第10周时达到了PASI75,而安慰剂组的相应数据为4%。
在研究II里,对于银屑病皮疹面积更广泛且接受过光疗的患者亚组,使用3mg/kg和 5mg/kg英夫利西单抗的患者有72%和77%在第10周时达到了PASI75,而安慰剂组的相应数据为2%。研究II里,对于银屑病皮疹面积更广泛,但不能耐受光疗或光疗治疗失败的患者,使用3mg/kg和5mg/kg英夫利西单抗的患者有70%和78%在第10周时达到了PASI75,而安慰剂组为2%。
在研究II中,研究者对3mg/kg和5mg/kg剂量组的292和297例英夫利西单抗治疗患者进行了有关疗效维持时间的评估。根据第10周的PASI疗效和研究地点对患者进行分层,自第14周开始,再次将本品治疗组的患者随机分为两组,让患者接受每8周维持治疗或按需治疗(PRN)。
相对于按需治疗的患者而言,每8周接受维持治疗的患者在50周达到PASI75比例更高,而且每8周给药5mg/kg组具有更好的疗效。图5显示了这些结果。英夫利西单抗的血清浓度在第46周降到谷底,在每8周给药组中,5mg/kg组有54%的患者达到PASI75,而3mg/kg组为36%。在每8周给药3mg/kg的患者中,达到PASI75的患者比例低于5mg/kg给药组,且可检测到的血清英夫利西单抗的患者比例也较低。
产生这种现象的部分原因可能与抗体产生率较高有关。此外,对于第10周取得疗效的患者,每8周输注5mg/kg英夫利西单抗可以让患者的疗效维持更长时间。无论是每8周维持治疗还是按需治疗,各患者亚组的疗效均有随时间下降的现象。在研究I为期50周的时间内,每8周使用5mg/kg英夫利西单抗的维持给药组所取得的结果与研究II的结果相似。
图5:至50周PASI从基线达到275%改善患者的比例(患者在14周时随机化)

未曾在斑块型银屑病患者中评价英夫利西单抗治疗超过50周的疗效和安全性。
溃疡性结肠炎
通过在接受传统治疗【口服糖皮质激素、氨基水杨酸盐和/或免疫调节剂(6-MP、AZA)]效果不佳的中重度活动性溃疡性结肠炎(UC)患者(Mayo评分6-12;内镜检查分项评分≥2)中开展的两项随机、双盲、安慰剂对照临床试验(ACT1和ACT2)评估了英夫利西单抗的安全性和有效性。允许稳定剂量的口服氨基水杨酸盐、糖皮质激素和/或免疫调节剂合并治疗。两项研究中,患者随机分配接受安慰剂、5mg/kg英夫利西单抗或10mg/kg英夫利西单抗,用药时间为第0、2、6、14和22周,以及ACT 1中第30、38和46周。第8周之后允许糖皮质激素减量。
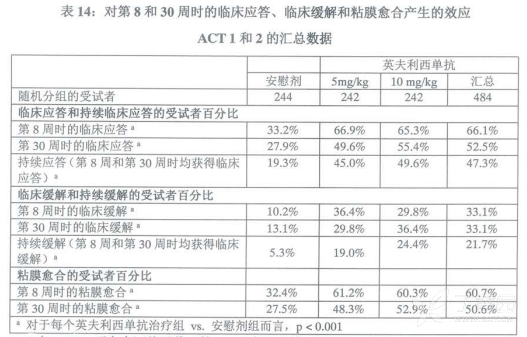
在ACT 1研究中评估了截至第54周时英夫利西单抗的有效性。第54周时,合并英夫利西单抗治疗组中44.9%的患者获得临床应答,与之相比安慰剂治疗组为19.8%(p<0.001)。第54周时合并英夫利西单抗治疗组中获得临床缓解和粘膜愈合的患者比例高于安慰剂治疗组(分别为34.6%vs.16.5%,p<0.001和46.1%vs.18.2%,p<0.001)。第54周时合并英夫利西单抗治疗组中获得持续应答和持续缓解的患者比例高于安慰剂治疗组(分别为37.9%vs.14.0%,p<0.001;和20.2%vs.6.6%,p<0.001)。
第30周(22.3%vs.7.2%,p<0.001,汇总ACT1和ACT2数据)和第54周(21.0%vs.8.9%,p=0.022,ACT 1数据)时,合并英夫利西单抗治疗组中能够在糖皮质激素停药的同时维持临床缓解的患者比例高于安慰剂治疗组。
从基线至第54周,对ACT 1和ACT 2研究及延长期所做的汇总数据分析显示,英夫利西单抗治疗后溃疡性结肠炎相关住院和外科手术减少。5mg/kg和10mg/kg英夫利西单抗治疗组的溃疡性结肠炎相关住院次数显著低于安慰剂组(每100受试者-年的平均住院次数:21和19次vs.安慰剂组40次;分别为p=0.019和p=0.007)。5mg/kg和10mg/kg英夫利西单抗治疗组的溃疡性结肠炎相关外科手术次数也低于安慰剂组(每100受试者-年的平均外科手术次数:22和19次vs.34次;分别为p=0.145和p=0.022)。
汇总ACT 1和ACT 2研究及延长期收集的研究药物首次输注后54周内任何时间接受结肠切除术的受试者比例。5mg/kg英夫利西单抗组(28/242或11.6%[无显著差异])和10mg/kg英夫利西单抗组(18/242或7.4%[p=0.011])中接受结肠切除术的受试者少于安慰剂组(36/244;14.8%)。
另外一项随机、双盲试验(C0168Y06)在静脉糖皮质激素治疗失败的中重度活动性溃疡性结肠炎且因此存在较高结肠切除术风险的住院患者(n=45)中评价了英夫利西单抗降低结肠切除术发生率的疗效。5mg/kg英夫利西单抗单次给药组的患者在研究输注后3个月内接受结肠切除术的患者显著少于安慰剂组(分别为29.2%vs.66.7%,p=0.017)。
在ACT 1和ACT 2中,疾病特异性量表IBDQ和通用36项目调査短表(SF-36)均显示有统计学意义的改善,证实英夫利西单抗可改善生命质量。
类风湿关节炎
经attract (合并用药治疗类风湿关节炎的抗tnf试验)和aspire (使用本品治疗类风湿关节炎早期发作的活性对照试验)两个多中心、随机、双盲临床试验,对本品的安全性和有效性进行了评价。在试验中可以合并使用稳定剂量的叶酸、糖皮质激素口服制剂(≤10mg/日)和/或非甾体抗炎药。终点的主要指标为根据美国风湿病学会(acr)标准评定症状和体征的减轻、预 防关节结构损害和改善身体机能。
在428名活动性类风湿关节炎患者(合用甲氨蝶呤)参加的安慰剂对照attract试验中,对第30、54和102周时的疗效进行了评价。入组患者的年龄中位值为54岁,患病期中位值为8.4年,肿胀关节数和触痛关节数中位值分别为20和31。约50%患者的身体机能为III级。患者被分为安慰剂组、3mg/kg英夫利西单抗组或10mg/kg英夫利西单抗组,分别于第0、2和6周给药,随后每隔4周或8周给药。全部患者在入组前均使用6个月稳定剂量的甲氨蝶呤(剂量中位值为15mg/周),并在试验过程中维持该稳定剂量。
Aspire试验评价了1004名未用甲氨蝶呤的早期(患病期<3年)活动性类风湿关节炎患者在第54周的疗效。入组患者年龄中位值为51岁,患病期中位值为0.6年,肿胀关节数和触痛关节数中位值分别为19和31。全部患者在第0、2和6周以及以后每8周时接受安慰剂、3mg/kg本品或 6mg/kg本品,同时合用甲氨蝶呤(在第8周前将剂量优化至20mg/周)。在上述试验中,前3次的输注时间应超过2小时,未出现严重输液反应的患者可以将之后的输注时间缩短,但不得少于40分钟。
临床疗效
症状和体征的减轻定义为在关节肿痛方面和以下5个标准中的3个都有至少20%的改善,即Acr20。这5个标准是:医师总体评定、患者总体评定、功能/残疾评估、视觉模拟疼痛量表、红细胞沉降率(esr)或c-反应蛋白(crp)。
在attract试验中,合用甲氨蝶呤的本品全部剂量及疗程组在54周中对症状和体征的改善均达到了美国风湿病学会标准的acr20(图1)。对症状和体征具有统计学意义的改善(acr20)可持续至第102周。
在attract试验中,英夫利西单抗组中达到acr50和acr70的患者多于安慰剂组(表3)。在获得显著疗效(定义为6个月维持acr70的效果)的患者比例上,英夫利西单抗组约为10%,而安慰剂组为0%(p<0.018)。
在aspire试验中,治疗54周后,在改善患者症状体征达到acr20、acr50和acr70的比例上,本品各剂量组均显著高于甲氨蝶呤单独用药组(表4)。在获得显著疗效的患者比例上,英夫利西单抗组为15%,而甲氨蝶呤单独用药组为8%(p=0.003)。
放射学检查显示的疗效
在第54周,通过放射学检查对手部和足部的关节结构损害(侵蚀及关节腔狭窄)进行Van Der Heijde-modified Sharp评分,该评分是对手/腕部和足部关节侵蚀数量和程度以及关节腔狭窄程度等结构损害进行评价的一种合成分数。
在attract试验中,约80%患者有放射学对照资料,结果列于表5。在第54周获得的具有统计学意义的防止关节损害发展的疗效可持续至第102周。
在aspire试验中,90%以上患者有至少2个可评价的放射学影像资料。在第30和54周(表6),可观察到本品+甲氨蝶呤合用组和甲氨蝶呤单用组对关节损害发展的抑制效果分别为97%和86%。在维持关节免于侵蚀的效果上(表7),本品+甲氨蝶呤合用组(79%)明显优于甲氨蝶呤单用组(57%)。在关节新生侵蚀的患者比例上(表8),本品+甲氨蝶呤合用组(47%)明显少 于甲氨蝶呤单用组(59%)。
身体机能的改善
在attract试验的102周中,在改善身体机能方面,本品+甲氨蝶呤的各剂量/疗程组的效果明显优于安慰剂+甲氨蝶呤组。经简明健康调查问卷(sf-36)对与健康相关的生活质量进行了评价。sf-36的8个次级评定并入2个总评分(身体总评分和精神总评分)。在102周中,本品+甲氨蝶呤的各剂量/疗程组与安慰剂+甲氨蝶呤组相比,显示了对身体总评分的明显改善,同时未对精神总评分产生不良影响(表9)。
在aspire试验的54周中,对于根据健康评定问卷评价的身体机能改善方面(表10),本品全部治疗组(0.7)的疗效显著优于甲氨蝶呤组(0.6),此差异具有统计学意义(p<0.001),同时未对sf-36精神总评分产生不良影响。
本品不与甲氨蝶呤合用的资料有限。
活动性克罗恩病
通过2项随机、双盲、安慰剂对照临床研宄在653名对传统治疗无充分应答的中度至重度活动性克罗恩病患者[克罗恩病活动指数(cdai)2220, S400]中评价了本品单剂量和多剂量的安全性和疗效。试验中允许伴随使用稳定剂量的氨基水杨酸盐、糖皮质激素和/或免疫调节制剂,92%的患者继续接受这些治疗中的至少1种药物。
在一项108名患者中进行的单剂量临床试验中,16% (4/25)的安慰剂组患者在第4周出现临床应答(cdai降低270),而5mg/kg本品组为81% (22/27)(p<0.001,双侧检验,fisher精确检验法)。另外,4% (1/25)的安慰剂组患者以及48%(13/27)的5mg/kg本品组患者在第4周 达到临床缓解(cdai<150)。
克罗恩病研宄I(accent I)多剂量临床试验中,545名患者在第0周接受一次5mg/kg本品,第2周出现临床应答的患者随机分至以下三个治疗组:安慰剂维持组在第2周、第6周及随后每8周给予安慰剂;5mg/kg维持组在第2周、第6周及随后每8周给予5mg/kg本品;10mg/kg维持组在第2周和第6周给予5mg/kg本品,随后每8周给予10mg/kg本品。对第2周出现临床应答的患者与未出现应答的患者分别进行随机分组,第6周后允许糖皮质激素减量。
第2周时,57% (311/545)的患者达到临床应答。第30周时,与安慰剂维持组相比,5mg/kg和10mg/kg维持组出现临床缓解的患者显著增多(表11)。
此外,在第54周,与安慰剂维持组相比,本品5mg/kg及10mg/kg维持组出现临床缓解且可停止使用糖皮质激素的患者比例更大(表11)。
本品维持组(5mg/kg和10mg/kg)患者与安慰剂维持组相比,应答维持时间更长(图2)。在第30周和第54周,5mg/kg和10mg/kg本品维持组与安慰剂维持组相比,疾病特异性炎性肠病调查问卷(ibdq)评分较基线明显改善,尤其是在肠道方面和系统改善方面更加明显,而且Sf-36中身体总评分也显著改善。
在基线出现黏膜溃疡且参与内窥镜研宄的78名患者中,第10周时,本品维持组13/43名患者内窥镜检查显示黏膜愈合,而安慰剂组1/28名患者达到黏膜愈合。第10周出现黏膜愈合的本品治疗患者中,9/12名患者在第54周也达到黏膜愈合。
获得应答但随后失去应答的患者将可接受比原随机分配剂量高出5mg/kg的本品治疗。这些患者多数能对较高剂量产生应答。在第2周未出现应答的患者中,59% (92/157)本品维持组患者在第14周出现应答,51% (39/77)安慰剂维持组患者出现应答。对于第14周未出现应答的患者,进一步治疗并未带来显著的临床应答。
瘘管性克罗恩病
通过2项在瘘管性克罗恩病成年患者(出现瘘管至少3个月)中进行的随机、双盲、安慰剂对照试验评价了本品的安全性和有效性。在研宄中,允许患者同时使用糖皮质激素、5-氨基水杨酸、抗生素、甲氨蝶呤、6-巯嘌呤和/或硫唑嘌呤。
在第1项试验中,有94名患者在第0、2和6周接受安慰剂或本品治疗。此项临床试验中观察到5mg/kg本品组(p=0.002)和10mg/kg本品组(p=0.021)瘘管应答(在未增加药物或手术治疗的情况下,在连续至少2次随访中,克罗恩病患者轻压有引流液的肠外瘘数量降低250%)的患者比例分别为68% (21/31)和56%(18/32),而安慰剂组为26%(8/31)。本品组患者显效时间中 位值和疗效持续时间中位值分别为2周和12周。本品组瘘管全部愈合的患者比例为52%,而安慰剂组的比例为13% (p<0.001)。
在第2项试验(accent Ii)中,入组的患者至少有一个引流性肠外瘘(肛周、腹部)。所有患者在第0、2和6周接受5mg/kg本品治疗。患者第14周随机分配至安慰剂或5mg/kg本品维持组。患者在第14周接受维持剂量治疗,随后每8周进行一次治疗,直到第46周。第10周和14周均获得瘘管应答(瘘管应答定义与第1项试验中相同)的患者与失去应答的患者分开进行随机。试验的终点为从随机分组直至应答消失的时间。
在所有随机分组的患者(从296名中初步纳入273名患者)中,87%有肛周瘘,14%有腹瘘,8%有直肠阴道瘘。高于90%的患者曾使用过免疫抑制剂或抗生素。
第14周时,65%(177/273)的患者出现瘘管应答。本品维持组的应答持续时间长于安慰剂维持组(图3)。第54周时,本品组无引流性瘘管的患者比例为38% (33/87),安慰剂组为22% (20/90)(p=0.002)。与安慰剂维持组相比,本品维持组患者存在住院次数减少的趋势。
获得应答但随后失去应答的患者将可接受比原随机分配剂量高出5mg/kg的本品治疗。安慰剂维持组患者给予5mg/kg本品后,66%(25/38)出现应答,57%(12/21)的本品维持组患者对10mg/kg剂量出现应答。
对于第14周未出现应答的患者,进一步治疗并未带来显著的临床应答。
各组出现新瘘管的患者比例相似(总体上达17%),出现脓肿的患者数量相似(总体上达15% )。
儿童活动性克罗恩病
初步的有效性资料来自于一项由21名基线时cdai中位值为322的儿童活动性克罗恩病患者(年龄11~17岁)参加的多中心、剂量盲法、单剂量、随机的药代动力学研宄,结果显示在剂量为1mg/kg、5mg/kg和10mg/kg时,本品可降低疾病的活动性。单剂量给药的临床效果出现于1周内,cdai平均降低112分,临床改善可持续8周,且耐受性良好。
强直性脊柱炎
一项对279例活动性强直性脊柱炎患者进行的随机、多中心、双盲、安慰剂对照研宄评价了本品的安全性和有效性。患者(年龄为18~74岁)入组标准符合修订版纽约标准对强直性脊柱炎 的定义。疾病处于活动期,bath强直性脊柱炎活动性指数(basdai)评分>4且脊柱痛>4[视觉模拟评分(vas)为0~10]。研宄排除了脊柱完全强直的患者,并且禁止使用改善病情抗风湿药(dmards)和全身用糖皮质激素。患者分别在第0、2、6、12和18周通过静脉给予剂量为5mg/kg的本品或安慰剂。
强直性脊柱炎症状和体征的改善情况通过asas (强直性脊柱炎评估)20疗效标准进行评价,在第24周,本品组和安慰剂组症状和体征改善达asas20疗效的患者比例分别为60°%和18°%(p<0.001)。此改善可在第2周被观察到,并且持续至第24周(图4和表12)。
在第24周,本品组达到asas50和asas70疗效的患者比例分别为44%和28%,而安慰剂组分别为9%和4%(p<0.001)。22%的本品组患者可达到低疾病活动状态[4个asas评估指标均<20 (分数范围是0~100mm)],而安慰剂组仅为1°% (p<0.001)。
与健康相关的生活质量经sf-36进行评价,与基线相比,第24周时本品组sf-36躯体功能总体评分改善的中位值为10.2,而安慰剂组为0.8 (p<0.001)。sf-36心理健康评分,本品组或安慰剂组均未发生变化。
此研宄结果与一项70例强直性脊柱炎患者进行的多中心、双盲、安慰剂对照研宄的结果相似。
斑块型银屑病
在评估英夫利西单抗安全性和有效性的3项随机、双盲、安慰剂对照研宄中,受试者为18岁及18岁以上的慢性、稳定性斑块型银屑病患者,其体表面积(bsa)210%且银屑病面积和严重程度指数评分(pasi)212,适合系统治疗或光疗。点滴状、红皮病型或脓疱型银屑病患者被排除。研宄期间不允许患者接受其它银屑病治疗,但在研宄开始10周之后可以在面部和腹股沟处使用弱效外用糖皮质激素。
研宄I(express)在378例适合接受光疗或系统治疗的斑块型银屑病患者中评价了英夫利 西单抗的诱导和维持疗法的有效性和安全性。患者在第0、2和6周输注5mg/kg英夫利西单抗或安慰剂,随后每8周接受一次维持治疗(安慰剂组至第22周;英夫利西单抗组至第46周)。在第24周时,安慰剂组患者交叉接受英夫利西单抗诱导治疗(5mg/kg),然后每8周接受一次维持 治疗。在46周内,最初被随机分配为接受本品治疗的患者继续每隔8周使用剂量为5mg/kg的英夫利西单抗。所有治疗组的基线pasi评分中位值为21,基线的静态医生整体评估(spga)为中度(52%的患者)、显著(36%的患者)、重度(2%的患者)。此外,75%患者的bsa>20%。 71%患者过去接受过系统治疗,82%接受过光疗。
研宄II(express II)评估了 835例接受安慰剂或3mg/kg和5mg/kg剂量英夫利西单抗患者 的有效性和安全性。在第0、2、6周的诱导期对他们进行评估。第14周时,将每个英夫利西单抗给药组的患者随机分为接受维持治疗的给药组(每8周给药一次)和按需要治疗的给药组(prn),治疗持续到46周。第16周时,安慰剂组交叉至英夫利西单抗诱导治疗组(5mg/kg),之后进入到每8周的维持治疗(5mg/kg)。在所有治疗组中,基线pasi评分中位值为18,63%患者的bsa>20%。55%的患者过去接受过系统治疗,64%的患者曾接受过光疗。
研宄III(spirit)评价了249例曾经接受过补骨脂素联合紫外线照射(puva)或其它系统治疗的银屑病患者。这些患者在第0、2、6周随机接受安慰剂或者剂量为3mg/kg或5mg/kg的英夫利西单抗治疗。在26周时,spga评分为中度或显著的患者(得分不低于3分,分数范围是0~5分)接受随机剂量的一次额外治疗。在所有治疗组中,基线pasi评分的中位值为19,基线 Spga的评分是中度(62%患者)、显著(22%)、严重(3%)。此外,75%患者的bsa>20%。入组研宄的患者中有114人(46%)在26周时使用了额外剂量的药物。
在研宄I、II和III中,在第10周时主要终点为达到pasi75 (pasi评分自基线改善75%)的 患者比例。在研宄I和研宄III中,另一种评价结果用spga评估包括达到清除或最轻患者的比例。spga是一种包含6个类别,评分范围从5=严重至0=清除来表示医生根据厚度、红斑和鳞屑来评估银屑病严重程度。治疗成功被定义为清除或最轻,包括无斑块突起或斑块突起很轻,皮疹呈淡红色,<5%的斑块上无或覆盖细小鳞屑。
研宄II还根据相对性医生整体评估(rpga)标准评估了达到清除或最小的患者百分比。Rpga以基线水平为基础,它包含6个类别,评分范围从6=严重至1=清除。总体病变的分级依据是皮疹面积占全身体表面积的百分比,以及厚度、鳞屑和红斑的程度。治疗成功被定义为清除或最轻,好转的标志是表现为粉红色或色素沉着的显著改善(接近正常的皮肤纹理;可能存在某些红斑),这些研宄的结果如表13所示。
研宄I里,对于银屑病皮疹面积更广泛且接受过光疗的患者亚组,使用5mg/kg英夫利西单抗的患者有85%在第10周时达到了 Pasi75,而安慰剂组的相应数据为4%。
研宄II里,对于银屑病皮疹面积更广泛且接受过光疗的患者亚组,使用3mg/kg和5mg/kg英夫利西单抗的患者有72%和77%在第10周时达到了 Pasi75,而安慰剂组的相应数据为2%。研宄II里,对于银屑病皮疹面积更广泛,但不能耐受光疗或光疗治疗失败的患者,使用3mg/kg和 5mg/kg英夫利西单抗的患者有70%和78%在第10周时达到了Pasi75,而安慰剂组为2%。
在研宄II中,研宄者对3mg/kg和5mg/kg剂量组的292和297例英夫利西单抗治疗患者进行了有关疗效维持时间的评估。根据第10周的pasi疗效和研宄地点对患者进行分层,自第14周开始,再次将本品治疗组的患者随机分为两组,让患者接受每8周维持治疗或按需治疗(prn)。
相对于按需治疗的患者而言,每8周接受维持治疗的患者在50周达到pasi75比例更高,而且每8周给药5mg/kg组具有更好的疗效。图5显示了这些结果。英夫利西单抗的血清浓度在第46 周降到谷底,在每8周给药组中,5mg/kg组有54%的患者达到pasi75,而3mg/kg组为36%。在每8周给药3mg/kg的患者中,达到pasi75的患者比例低于5mg/kg给药组,且可检测到的血清英夫利西单抗的患者比例也较低。
产生这种现象的部分原因可能与抗体产生率较高有关。此外,对于第10周取得疗效的患者,每8周输注5mg/kg英夫利西单抗可以让患者的疗效维持更长时间。无论是每8周维持治疗还是按需治疗,各患者亚组的疗效均有随时间下降的现象。在研宄i为期50周的时间内,每8周使用5mg/kg英夫利西单抗的维持给药组所取得的结果与研宄II的结果相似。
未曾在斑块型银屑病患者中评价英夫利西单抗治疗超过50周的疗效和安全性。
遗传毒性
在小鼠体内微核试验或鼠沙门氏菌-大肠杆菌(Ames)实验中,未发现本品有致突变性。在人体淋巴细胞进行的试验中未观察到染色体畸变。尚不知这些发现对人体的意义。
生殖毒性
cV1q是一种与本品类似的抗体,可以抑制小鼠体内TNFa的活性。釆用cV1q进行的生育力和一般生殖毒性研究中,未观察到其对动物生育力的影响。尚不清楚注射用英夫利西单抗是否损害人的生育力。
致癌性
利用接受cV1q抗小鼠TNFa的抗体的小鼠进行的一项重复剂量毒理学研究,以对该抗体的致癌性进行了评价。小鼠分为3组,每周分别接受对照品、cV1ql0mg/kg、40mg/kg,持续6个月,每周10mg/kg和40mg/kg的剂量显示cV1q未对小鼠中产生致癌性。