印度 Vemurafenib Zelboraf 240mg 维罗菲尼 维罗非尼 威罗菲尼 威罗飞尼 维莫非尼片 佐博伏 威罗非尼
转移性黑色素瘤
| 数量: | 库存 100 件 |
中文名:威罗菲尼
商品名:Zelboraf
英文名:Vemurafenib
规 格:240mg
生产厂家:Roche罗氏制药
威罗菲尼.Zelboraf 在2011年8月份被FDA批准用于治疗晚期转移性或不能切除的黑色素瘤;2012年2月20日,欧盟委员会批准其用于治疗成人BRAF V600突变阳性、经手术不能切除或转移性黑色素瘤。
使用限制:有野生型BRAF黑色素瘤患者中建议不使用威罗菲尼.ZelborafF。
【使用方法】
推荐剂量:960 mg口服。
约12小时间隔壹次。
吞服, 不应咀嚼或压碎。
症状性不良药物反应的处理可能需要减低剂量,中断治疗,或终止ZELBORAF治疗。不建议减低剂量导致剂量低于480 mg。
【不良反应】
最常见不良反应(≥ 30%)是关节痛,皮疹,脱发,疲乏,光敏反应,恶心,瘙痒和皮肤乳头状瘤。
【特殊人群中使用】
哺乳母亲:当接受ZELBORAF时终止哺乳
【警告&注意事项】
(1)24%患者中发生皮肤鳞状细胞癌(cuSCC)。治疗开始前和当用治疗时每2个月进行皮肤学评价。切除处理和继续治疗不调整剂量。
(2)治疗期间和再次开始治疗时曾报道严重超敏反应,包括过敏反应。经受严重超敏反应患者中终止威罗菲尼.ZelborafF。
(3)曾报道严重皮肤学反应,包括Stevens-Johnson综合征和中毒性表皮坏死溶解。经受严重皮肤学反应患者中终止治疗。
(4)曾报道QT延长。治疗前和调整剂量后监视ECG和电解质。在第15天,治疗头3个月期间每3个月,其后每3个月,或更常如临床指示时监视ECGs。如QTc超过500 ms,短暂中断ZELBORAF,校正电解质异常,和控制 对QT延长风险因子。
(5)可能发生肝实验室异常。治疗开始前和治疗期间每月,或当临床指示时监视肝酶和胆红素。
(6)曾报道光敏性。服用ZELBORAF时建议患者避免暴露阳光。
(7)曾报道严重眼科反应,包括葡萄膜炎,虹膜炎和视网膜静脉阻塞。对眼科反应常规监视患者。
(8)曾报道新原发性恶性黑色素瘤。切除处理,和继续治疗无剂量调整。如上所述,进行皮肤学监视。
(9)妊娠:可能致胎儿危害. 忠告妇女对胎儿潜在风险.
(10)为了选择适于ZELBORAF治疗患者,用壹种FDA-批准的检验BRAF突变。尚未在有野生型BRAF黑色素瘤患者中研究ZELBORAF的疗效和安全性。
以上信息谨供参考, 医药使用相关事项, 请与妳的专业医生咨询
患者必须经由CFDA批准的检测方法确定的证明肿瘤为BRAFV600 突变阳性,才可使用维莫非尼治疗。维莫非尼不能用于BRAF野生型黑色素瘤患者。
标准剂量
维莫非尼的推荐剂量为960mg(四片240mg片剂),每日两次。首剂药物应在上午服用,第二剂应在此后约12小时,即晚上服用。每次服药均可随餐或空腹服用。
用一杯水送服药物,服药时整片吞下维莫非尼片剂。不应咀嚼或碾碎维莫非尼片剂。
治疗持续时间
建议维莫非尼治疗应持续至疾病进展或发生不可接受的毒性反应(参见表1和表2)。
漏服
如果漏服一剂药物,可在下一剂服药4小时以前补服漏服的药物,以维持每日两次的给药方案。不应同时服用两剂药物。
呕吐
如果维莫非尼服药后发生呕吐,患者不应追加剂量,而应按常规剂量继续治疗。
剂量调整 (参见【注意事项】和【不良反应】)
对于伴有症状的不良事件或QTc间期延长的处理,可能需要按照表1或表2降低剂量、暂时中断用药或停止维莫非尼治疗。对于出现皮肤鳞状细胞癌(cuSCC)不良事件,不建议调整剂量或中断用药。不建议采用低于480mg每日两次的剂量。
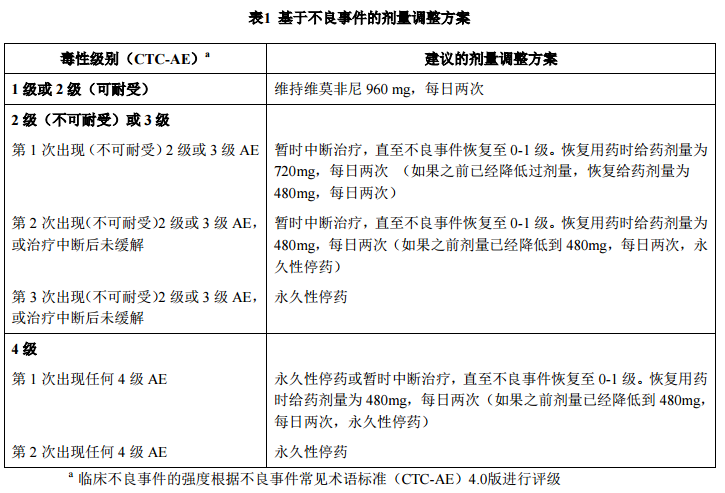
一项在既往接受过治疗的转移性黑色素瘤患者中开展的非对照、开放II期临床研究中观察到暴露-依赖的QT延长。对于QTc延长的管理可能需要特定的监测手段(参见【注意事项】)。

*特殊人群剂量说明 * 老年人:对于年龄≥65岁的患者,无特殊剂量调整需求。
儿童:维莫非尼对18岁以下患者的安全性和有效性尚未确立。维莫非尼未批准用于18岁以下的患者(参见【药代动力学】)。
肾功能受损:对于轻度或中度肾功能受损的患者,无需进行起始剂量调整(参见【药代动力学】)。对于重度肾功能受损的患者,由于数据不足,无法确定是否需要进行剂量调整。
肝功能受损:对于轻度或中度肝功能受损的患者,无需进行起始剂量调整(参见【药代动力学】)。对于重度肝功能受损的患者中,由于数据不足,无法确定是否需要进行剂量调整。
临床试验中的不良反应
安全性特征总结
维莫非尼的临床开发研究项目作为一个整体项目进行分析时,预估共6300例患者接受过维莫非尼治疗。
患有不可切除或转移性黑色素瘤的患者:
药物不良反应(ADR)来自2项临床试验,一项为在初治的 BRAFV600突变阳性的不可切除或转移性黑色素瘤患者(N=675)中进行的III期临床研究(NO25026),另一项为在至少一次既往系统性治疗失败的BRAFV600突变阳性的转移性黑色素瘤患者(N=132)中进行的II期临床研究(NP22657)。
在III期开放性研究(NO25026)中,被随机分配至维莫非尼组的患者接受每日2次口服,起始剂量为960mg;被随机分配至阳性对照组的患者接受1000mg/m2的达卡巴嗪治疗,采用静脉途径给药,每3周一次。维莫非尼中位治疗时间6.6个月,与此相比,达卡巴嗪的中位治疗时间0.8个月。II期临床研究(NP22657)是一项开放性、非对照、单组研究。在这项研究中,患者接受维莫非尼 960mg每日两次的治疗,中位治疗时间5.7个月。
最常见的任意级别ADR(任一研究≥30%)为关节痛、疲乏、皮疹、光敏反应、脱发、恶心、腹泻、头痛、瘙痒、呕吐、皮肤乳头状瘤和皮肤角化症。最常见(≥5%)3级ADR为cuSCC、角化棘皮瘤、皮疹、关节痛和γ-谷氨酰转移酶(GGT)升高。两项研究中4级不良反应的发生率均≤4%。研究NO25026中导致研究药物永久停用的不良事件的发生率为7%。研究NP22657中,导致研究药物永久停用的不良事件的发生率为 3%。
下表3总结了患有不可切除或转移性黑色素瘤患者的ADR。ADR均按MedDRA系统器官分类列出。各种ADR的相应发生频率分类基于以下规定:十分常见(≥1/10);常见(≥1/100至<1/10);不常见(≥1/1,000 至<1/100);罕见(≥1/10,000至<1/1,000);十分罕见(<1/10,000)。

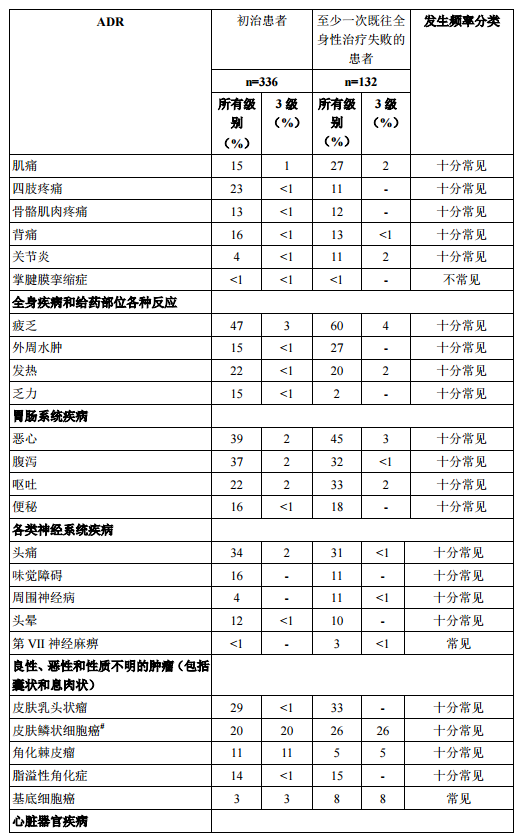
*有关来自临床试验的选定不良反应的信息 *
皮肤鳞状细胞癌(cuSCC)(参见【注意事项】)
在各研究中,对于不可切除或转移性黑色素瘤接受维莫非尼治疗的患者,皮肤鳞状细胞癌的发生率约为20%。在由一个独立中心皮肤病实验室审核的结果显示:其中绝大多数切除病变被归类为SCC-角化棘皮瘤亚型或具有混合性角化棘皮瘤特征的亚型(52%),两者均为较良性、侵袭性较小的皮肤鳞状细胞癌类型。大多数归类为“其他”的病变(43%)为良性皮肤病变(例如,寻常疣、光化性角化病、良性角化病、囊肿/良性囊肿)。皮肤鳞状细胞癌通常发生于治疗早期阶段。对于发生cuSCC的患者,中位发生时间范围为 7.1至8.1周。在发生皮肤鳞状细胞癌的患者中,约33%的患者的发生次数大于一次,其中两次发作之间的中位间隔时间为6周。对于皮肤鳞状细胞癌病例,通常采用简单切除的处理方式,并且患者一般能继续接受治疗,不需要剂量调整。
超敏反应(参见【注意事项】)
在一项临床试验中,维莫非尼960mg每日两次的给药方案治疗8天后,发生一例超敏反应病例,表现为皮疹、发热、寒战和低血压。重新开始维莫非尼治疗,单次给药240mg后又观察到类似症状。该患者永久性停止维莫非尼治疗,并恢复正常,且未留下任何后遗症。
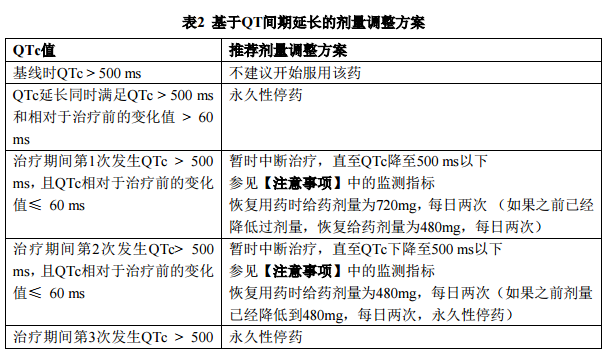
QT间期延长(参见【注意事项】)
一项开放性、非对照、II期、QT子研究(132名患者接受维莫非尼治疗,960mg每日两次)所得的中心心电图分析结果显示,与基线相比,QTc间期平均延长值从第1天(3.3ms,95%置信区间上限:5ms)至第15天(12.8ms,95%置信区间上限:14.9 ms)有所增加。
在这项研究中,观察到药物暴露依赖性QTc间期延长,并且平均 QT间期延长效应在第一个月治疗之后保持稳定,数值在12至15ms之间,在治疗的前6个月内可观察到最大平均QTc间期延长(15.1ms;95%置信区间上限:17.7ms)(n=90名患者)。两名患者(1.5%)在治疗中出现绝对QTc值大于500ms(CTCAE3级),但仅一名患者(0.8%)的QTc间期相对基线水平的变化值大于60ms。
对QT间期延长的建模和模拟得到以下估计值:对于960mg,每日两次给药方案,QTcP间期延长幅度超过60ms的患者百分比预计为 0.05%。对于体重指数为45kg/m2的肥胖患者,预计该百分比提高至0.2%。QTcP相对基线水平的变化值大于60ms的患者百分比预计为0.043%(男性)和0.046%(女性)。QTcP间期值大于 500ms的患者百分比预计为0.05%(男性)和1.1%(女性)。
实验室检查异常
患有不可切除或转移性黑色素瘤的患者III期临床研究(NO25026)中,肝功能实验室检查异常结果(从基线正常升高至 3级或4级的患者比例)总结见表4。
:
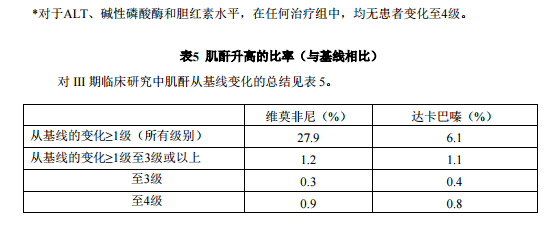
*上市后经验 *
基于自发性病例报告和参考文献病例,已在维莫非尼的上市后经验中发现以下药物不良反应(表6)。 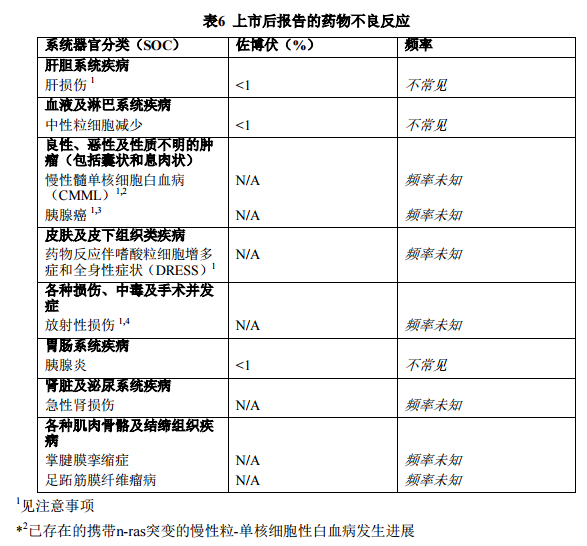

上市后有关不良反应的更多信息
急性肾脏损伤
应用维莫非尼患者中已经有报告轻重程度不一的肾脏不良反应,包括从轻中度肌酐升高,到急性间质性肾炎和急性肾小管坏死,部分病例是在脱水情况下观察到的。大多数情况下,肌酐升高似乎可自然逆转(参见【注意事项】)。
*实验室异常 *
肝功能实验室异常包括ALT≥5倍正常上限、ALP≥2倍正常上限和ALT≥3倍正常上限并伴随胆红素浓度升高(>2倍正常上限),这些异常在上市后已有报告(参见【注意事项】)。
上市后有报告肌酐实验室检查异常的病例(参见【注意事项】)。
概述
服用本品前,患者必须获得经充分验证的检测方法证实的 BRAF V600 突变阳性肿瘤评估结果。
恶性肿瘤
皮肤鳞状细胞癌(cuSCC)
在接受维莫非尼治疗的患者中,已报告皮肤鳞状细胞癌病例(包括被归类为角化棘皮瘤或混合型角化棘皮瘤亚型的病例)(参见【临床试验】和【不良反应】)。皮肤鳞状细胞癌通常发生于治疗早期。在维莫非尼临床试验中,与皮肤鳞状细胞癌相关的潜在风险因素包括年龄(≥65岁)、既往皮肤癌和长期日光暴露。皮肤鳞状细胞癌病例通常采用简单切除加以处理,且患者能够继续治疗,不需要剂量调整。
建议所有患者在开始治疗前接受一次皮肤评估,并且建议在治疗过程中接受常规监测。对于任何可疑皮肤病变,均应切除,对标本进行皮肤病理评估,并按照当地标准进行治疗。
维莫非尼停药后,监测应持续6个月,或直至开始另一种抗肿瘤治疗。
应指导患者将发生的任何皮肤改变通知其医师。
非皮肤鳞状细胞癌(非cuSCC)
已收到接受维莫非尼治疗的患者发生非皮肤鳞状细胞癌的报告。患者应接受头部和颈部检查,其中应包含治疗开始前的至少一次口腔粘膜视诊和淋巴结触诊,并在治疗期间每3个月检查一次。此外,患者在开始治疗前还应接受一次胸部CT扫描,并在治疗期间每6个月接受一次扫描。在治疗前和治疗结束时,或有临床指征时,建议进行盆腔检查(针对女性)和肛门检查。
维莫非尼停药后,对非皮肤鳞状细胞癌的监测应持续至6个月,或直至开始另一种抗肿瘤治疗。若有临床指征时应对检查发现的异常进行评估。
新发原发性黑色素瘤
在临床试验中,已报道新发原发性黑色素瘤。病例的处理方式为切除,患者继续接受治疗,而不需要调整剂量。应根据以上针对皮肤鳞状细胞癌的原则对皮肤病变进行监测。
其他恶性肿瘤
基于其作用机制,维莫非尼可引起与RAS突变相关的癌症进展(参见【不良反应】)。
对于既往发生或合并发生RAS突变相关癌症的患者,应谨慎使用维莫非尼。
BRAF野生型黑色素瘤的肿瘤进展
体外研究显示BRAF野生型细胞暴露于BRAF抑制剂时MAP激酶信号传导激活和细胞增殖增加。在开始维莫非尼治疗前,需确定 BRAFV600突变阳性。维莫非尼不能用于BRAF野生型黑色素瘤患者。
胰腺炎
接受维莫非尼治疗的患者已有发生胰腺炎的报道,但不常见。其严重程度大多为轻中度。
发生未知原因的腹痛时应及时进行检查(包括血清淀粉酶和脂肪酶的检查),确诊胰腺炎后应根据当地诊疗常规给予积极治疗。患者在胰腺炎发作后,若重新接受维莫非尼治疗,应对其进行密切监测。
超敏反应
已有报告与维莫非尼治疗相关的严重超敏反应,包括全身性过敏反应(参见【禁忌】和【不良反应】)。重度超敏反应包括:全身性皮疹和红斑或低血压。对于发生重度超敏反应的患者,应永久性停止维莫非尼治疗。
皮肤反应
研究报告显示,接受维莫非尼治疗的患者中已经有重度皮肤反应的发生,其中包括在关键性临床试验中出现的罕见的Stevens-Johnson综合征和中毒性表皮坏死溶解。与维莫非尼相关的药物反应伴嗜酸粒细胞增多症和全身性症状(DRESS)已有报告(参见【不良反应】)。
对于发生重度皮肤反应的患者,应永久性停止维莫非尼治疗。 放射性毒性增强接受维莫非尼治疗前后或治疗过程中还接受放疗的患者中,已有放射治疗回忆反应和放疗增敏作用的病例报道(参见【药物相互作用】和【不良反应】上市后经验)。
大多数属于皮肤性病例,但有一些累及内脏器官导致死亡的病例。在同步或序贯给予放射治疗时,应谨慎使用维莫非尼。
QT间期延长
在一项既往接受治疗的转移性黑色素瘤患者的非对照、开放性、II期、QT子研究中,观察到暴露依赖性QT间期延长(参见【不良反应】)。QT间期延长可导致室性心律失常的风险升高,包括尖端扭转型室性心动过速。对于存在无法纠正的电解质异常、长QT综合征或正在服用已知能延长QT间期的药物的患者,不建议采用维莫非尼治疗。
在维莫非尼治疗前和剂量调整后,应监测心电图和电解质。治疗的前3个月应每月监测,此后每3个月进行一次监测,或根据临床指征的需要适当增加监测频率。
对于QTc>500ms的患者,不建议开始维莫非尼治疗。如果治疗期间QTc超过500ms(CTCAE≥3级),应暂时中断维莫非尼治疗,纠正电解质异常,并且应对QT间期延长的心脏风险因素加以控制(例如,充血性心力衰竭,心动过缓)。应在QTc间期下降至500ms以下后才考虑重新开始治疗,并降低剂量水平,如表1和表2中所述。如果相关风险因素纠正后,QTc仍大于500ms,且相对于治疗前数值的变化大于60ms,则建议永久性停用维莫非尼治疗。
肝损伤
在维莫非尼的研究中,已报告肝损伤病例,包括重度肝损伤病例(参见【不良反应】)。
维莫非尼治疗过程中可发生肝功能实验室异常(参见【不良反应】)。在开始治疗之前,应监测肝酶水平(转氨酶和碱性磷酸酶)和胆红素水平,在治疗过程中,应每月监测一次,或根据临床需要确定监测频率。对于实验室异常,应酌情采用减量、治疗中断或停止治疗的方式加以处理(参见【用法用量】)。
光敏反应
根据临床试验报告,在接受维莫非尼治疗的患者中出现轻度至重度的光敏反应(参见【不良反应】)。应建议所有患者在服用维莫非尼期间避免日光暴露。在服用药物期间,应建议患者穿戴防护性服装,并在室外使用广谱UVA/UVB防晒霜和润唇膏(SPF≥30),有助于在日晒环境下保护患者。
对于2级(不可耐受)或更高级别不良事件的光敏反应,建议调整剂量(参见【用法用量】)。
掌腱膜挛缩症和足跖筋膜纤维瘤病
维莫非尼用药期间曾有掌腱膜挛缩症和足跖筋膜纤维瘤病报告。大部分病例的严重程度为轻度至中度,但是也有重度、导致残疾的掌腱膜挛缩症的病例报告(参见【不良反应】)。
对于这类不良反应,应酌情采用减量、中断治疗或停止治疗的方式处理(参见【用法用量】)。
眼部反应
已报告的严重眼部反应包括葡萄膜炎。应定期监测患者是否发生某些眼部不良反应(参见【不良反应】)。
与ipilimumab的联合用药
在一项 期临床试验中,ipilimumab(3mg/kg)与维莫非尼(960mg,每日两次或720mg,每日两次)联合用药,报道了无症状性3级转氨酶和胆红素水平升高。基于这些数据,不建议 ipilimumab与维莫非尼联合用药。
药物滥用和药物依赖性
无
驾驶和操作机器的能力
尚不清楚本品对驾驶和操作机器能力的影响。患者应意识到疲劳或眼睛问题可能会影响驾驶车辆。
其它特殊人群中的应用
性别
在报告的 3 级不良事件中,女性患者比男性患者在皮疹、关节痛和光敏反应上更多见(参见【药代动力学】)。
肾功能受损
对于肾功能受损的患者,可用数据有限。在重度肾功能受损的患者中,无法排除增加血药浓度所带来的风险(参见【用法用量】和【药代动力学】)。
肝功能受损
对于肝功能受损的患者,可用数据有限。由于维莫非尼通过肝脏清除,重度肝功能受损患者的血药浓度水平可能升高(参见【用法用量】和【药代动力学】)。
实验室检查 肝功能检查
肝脏实验室异常可能伴随维莫非尼的使用发生(转氨酶、碱性磷酸酶和胆红素升高),参见【注意事项】中概述和【不良反应】中实验室检查异常。
在开始治疗之前应监测肝酶水平,且在治疗过程中应每月监测一次,或根据临床需要确定监测频率。对于剂量调整参见【用法用量】。
肌酐
已报告实验室异常病例,大多数病例为轻度(>1-1.5倍ULN)或中度(>1.5–3倍ULN)肌酐升高。大多数情况下,肌酐升高是可逆的(参见【不良反应】)。在开始治疗前,应检测血清肌酐水平,在治疗过程中,应根据临床需要定期监测。对于实验室异常,应酌情采用减量、治疗中断或停止治疗的方式加以处理(参见【用法用量】)。
维莫非尼对药物代谢酶的影响在转移性黑色素瘤患者中进行的体内药物-药物相互作用研究结果证明,维莫非尼是一种中度CYP1A2 抑制剂和CYP3A4诱导剂。
不建议维莫非尼与经CYP1A2和CYP3A4代谢的治疗窗较窄的药物联合应用。如果无法避免联合用药,应谨慎,因为维莫非尼可使 CYP1A2底物的血浆暴露量升高,也可使CYP3A4底物的血浆暴露量降低。根据临床需要可考虑降低合并CYP1A2底物的剂量。一项临床试验中,维莫非尼联合用药导致咖啡因(CYP1A2底物)的AUC 升高了2.6倍,咪达唑仑(CYP3A4底物)的AUC降低了39%。另一项临床试验中,维莫非尼治疗导致2mg单次用药替托尼定(CYP1A2底物)的AUClast和AUCinf分别升高约4.2倍和4.7 倍。
美沙芬(CYP2D6底物)及其代谢产物右啡烷的AUC升高了47%,显示维莫非尼对美沙芬的动力学的影响,可能不是通过CYP2D6抑制作用介导的。
维莫非尼与S-华法林(CYP2C9 底物)的联合用药导致S-华法林的AUC升高18%(参见【药代动力学】)。在维莫非尼与华法林联合用药的情况下,应谨慎,并考虑额外的INR(国际标准化比值)监测。
在体外试验中,维莫非尼中度抑制CYP2C8。该研究的体内相关性目前未知,但不能排除联合使用CYP2C8底物可能产生临床相关效应的风险。对于维莫非尼与治疗窗口较窄的CYP2C8底物的联合应用,应保持谨慎,因为维莫非尼可能导致其血药浓度升高。
抑制或诱导CYP3A4的药物
维莫非尼是CYP3A4的底物,因此,与强效CYP3A4抑制剂或诱导剂的联合应用可改变维莫非尼的血药浓度。与强效CYP3A4诱导剂利福平联合应用能显著降低维莫非尼的血浆暴露量(AUC),使单次给予960mg维莫非尼后的血浆暴露量下降约40%(参见【药代 动力学】)。在与维莫非尼联合用药的情况下,应慎用强效 CYP3A4抑制剂(例如,酮康唑、伊曲康唑、克林霉素、阿扎那韦、奈法唑酮、沙奎那韦、泰利霉素、利托那韦、茚地那韦、 奈非那韦、伏立康唑)和诱导剂(例如,苯妥英、卡马西平、利福平、利福布汀、利福喷汀、苯巴比妥)。
放射治疗
已报告患者接受维莫非尼治疗过程中发生放疗毒性增强的病例(参见【注意事项】和【不良反应】)。绝大多数患者接受了大于或等于2Gy/天的放疗方案(大分割方案)。
维莫非尼与药物转运系统的相互作用
体外研究证明,维莫非尼既是外排性转运蛋白P-糖蛋白(P-gp)和乳腺癌耐药蛋白(BCRP)的底物,也是这两种蛋白的抑制剂。 使用P-gp底物药物(地高辛)进行的临床药物相互作用研究 GO28394表明,多次口服维莫非尼(960mg,每日两次)可增大单次口服剂量地高辛的暴露量,地高辛AUCAUClast和 Cmax约分别增加1.8倍和1.5倍。在维莫非尼与P-gp底物合并给药时应谨慎。
根据临床需要可考虑降低合并P-gp底物药物的剂量。
维莫非尼对BCRP底物药物的影响以及BCRP诱导剂和抑制剂对维莫非尼血药浓度的影响目前未知。
体外研究还证明,维莫非尼是胆汁酸盐输出泵的一种抑制剂。该研究发现的体内相关性目前未知。
国外研究
已在一项III期临床研究的675名患者和两项II期临床试验的278 名患者中评价了维莫非尼的疗效。进入研究前,对所有患者的肿瘤样本采用cobas®4800BRAFV600突变检测是否存在BRAFV600突变。
初治患者
一项开放性、国际多中心、随机III期临床研究支持维莫非尼应用于初治BRAFV600突变阳性的不可切除或转移性黑色素瘤患者。患者被随机分配至维莫非尼治疗组(960mg,每日两次)或达卡巴嗪治疗组(1000mg/m2,每3周一次)。
总计675名患者被随机分配至维莫非尼治疗组(n=337)或达卡巴嗪治疗组(n=338)。
随机入组时,根据疾病分期、乳酸脱氢酶(LDH)、ECOG体能状态和地理区域分层。各治疗组之间基线特征分布均衡。对于随机分配至维莫非尼治疗组的患者,多数患者为男性(59%)和高加索人种(99%),中位年龄为56岁(28%的患者≥65岁),所有患者的 ECOG体能状态为0或1分,绝大多数患者存在M1c期疾病(66%)。研究的共同-主要疗效终点为总生存期(OS)和无进展生存期(PFS)。关键次要终点包括经确认的最佳总体缓解率(BORR) 和缓解持续时间。
在预先定义的中期分析(截止日期为2010年12月30日)时,对于共同主要终点总生存期(OS)(p<0.0001)和无进展生存期(PFS)(p<0.0001)均观察到具有统计学意义及临床意义的改善(非分层对数秩检验)。在此后3个月更新分析时(截止日期为 2011年3月31日),总计有200名患者死亡(78名来自维莫非尼治疗组,122名来自达卡巴嗪治疗组)。
OS的中位随访时间在维莫非尼治疗组为6.2个月(范围在0.4至13.9个月之间),在达卡巴嗪治疗组为4.5个月(范围在小于 0.1至11.7个月之间)。维莫非尼治疗组的总生存期长于达卡巴嗪治疗组,风险比为0.44(95%置信区间:0.33,0.59),表示接受维莫非尼治疗的患者相比接受达卡巴嗪治疗的患者死亡风险下降 56%。维莫非尼治疗组6个月生存率的Kaplan-Meier(K-M)估计值为83%(95%置信区间:79%,87%),达卡巴嗪治疗组为63% (95%置信区间:57%,69%)。截至分析时,维莫非尼治疗组中位OS的K-M估计值尚未达到(95%置信区间:9.6,未达到),达卡巴嗪治疗组的中位OS为7.9个月(95%置信区间:7.3,9.6)。
在最后一名患者随机入组后24个月,对OS进行了一项更新的事后分析(截止日期2012年12月20日)。此次分析时,已有478名患者死亡242名来自维莫非尼治疗组,236名来自达卡巴嗪治疗组)。维莫非尼治疗组的中位随访时间为13.4个月(范围:0.4 至 33.3个月)。
维莫非尼组的中位OS的K-M估计值为13.6个月(95%置信区间:12.0,15.3)。
由研究者评估的无进展生存期(PFS)在维莫非尼治疗组长于达卡巴嗪治疗组,风险比为0.26(95%置信区间:0.20,0.33),表示接受维莫非尼治疗的患者相对接受达卡巴嗪治疗的患者进展或死亡的风险下降74%。维莫非尼治疗组中,6个月PFS率的Kaplan-Meier(K-M)估计值为47%(95%置信区间:38%,55%),而达卡巴嗪治疗组的相应数据为12%(95%置信区间:7%,18%)。在维莫非尼治疗组中,中位PFS为5.32个月(95%置信区间:4.86,6.57),而达卡巴嗪治疗组的中位PFS为1.61个月(95%置信区间:1.58,1.74)。对于次要终点,由研究者评估的经确认的最佳总体缓解率(CR+PR),维莫非尼治疗组患者(48.4%)(95%置信区间:41.6%,55.2%)较达卡巴嗪治疗组(5.5%)(95%置信区间:2.8%,9.3%)有显著提高(p<0.0001)。在37%的维莫非尼治疗组患者和24%的达卡巴嗪治疗组患者中,观察到基于RECIST1.1判定的疾病稳定。
在各亚组(年龄、性别、基线LDH、ECOG体能状态、转移性疾病分期)与地理区域中,均可观察到有利于维莫非尼治疗组的OS、PFS和经确认的最佳总体缓解率的改善。
疗效结果见表7、图1(更新OS)和图2(PFS)。 


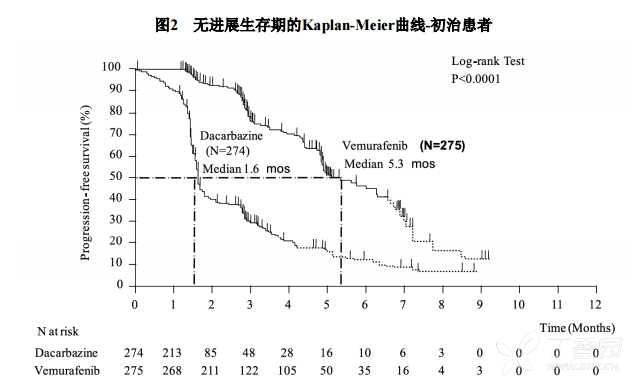
在有体能状态改善(基于医师评价)的患者比例方面,维莫非尼治疗组(63.4%)(95%置信区间:57%,69%)高于达卡巴嗪治疗组(20.2%)(95%置信区间:15%,26%)。
对NO25026试验中673名患者的肿瘤样本进行回顾性测序,其中57名患者报告为BRAFV600K突变阳性黑色素瘤。尽管患者数量较少,疗效分析结果显示维莫非尼用于这些V600K突变阳性肿瘤患者在OS、PFS和证实的总体最佳缓解方面均有相似的临床获益。
既往至少有一次系统性治疗失败的患者
在至少接受过一次既往治疗的转移性黑色素瘤患者中进行的一项 II期、单组、国际多中心研究中,N=132患者中位年龄为52岁,其中19%的患者年龄大于65岁。大多数患者为男性(61%),高加索人种(99%),疾病分期为M1c(61%)。49%的患者既往治疗失败的次数≥2。中位随访时间为6.87个月(范围0.6至11.3个月之间)。
主要终点-经确认的最佳总体缓解率(CR+PR)(由独立审查委员会(IRC)评估)为52%(95%置信区间:43%,61%)。中位至疾病缓解时间为1.4个月,其中75%的疾病缓解发生于治疗第1.6个月时。由IRC评估的缓解持续时间的中位值为6.5个月(95%置信区间:5.6,未达到)。在30%的患者中,观察到基于RECIST1.1判定的疾病稳定。中位总生存期为15.9个月(95%置信区间:11.2,19.3),6个月生存率为77%(95%置信区间:69%,84%),1年存率为58%(95%置信区间:48%,66%)。中位PFS 为6.1个月(95%置信区间:5.5,6.9),6个月PFS率为52%(95%置信区间:43%,61%)。
脑转移患者
在经组织学确认为BRAFV600突变阳性转移性黑色素瘤并有脑转移的成年患者中进行了一项开放性、单臂、多中心、II期维莫非尼研究(N=146)。这项研究包括两个同时入组的队列:
既往未经治疗患者(队列1:N=90):患者既往未接受过针对脑转移的治疗;允许既往接受过针对转移性黑色素瘤系统性治疗。 既往经治疗患者(队列2:N=56):患者既往接受过针对脑转移的治疗,并且在治疗后疾病发生进展。对于接受过立体定向放射治疗(SRT)或手术治疗的患者,必须在这项既往治疗后出现了新的 RECIST-可评估的脑部病灶。
患者的中位年龄为54岁(范围是26-83岁),且两个队列的中位年龄相似。大多数患者为男性(61.6%),两个队列间的性别分布相似。报告共135例患者(92.5%)为白人,因当地法规原因,11 例患者的种族(7.5%)未报告。两个队列在基线时的脑部靶病灶中位数目为2(范围是1-5)。
该研究的主要目的为评估在患有脑转移且既往未经治疗的转移性黑色素瘤患者中维莫非尼的疗效,依据脑部的最佳总体缓解率(BORR),由独立审查委员会(IRC)使用《实体瘤治疗疗效评价标准》版本1.1(RECISTv1.1)进行评估。
次要目的包括评估在既往接受过治疗的患者脑部的BORR、脑转移患者的治疗缓解持续时间(DOR)、无进展生存期(PFS)和总体生存期(OS),以评价维莫非尼的疗效。
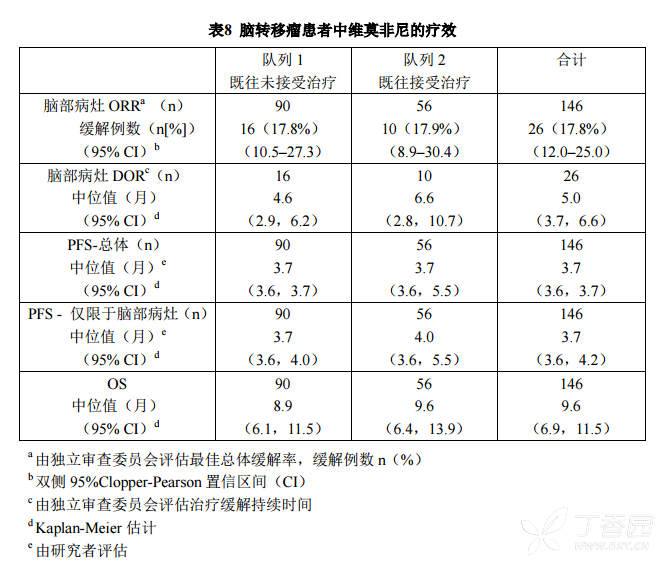
**中国研究
YO28390**
YO28390是一项开放性、单臂、多中心、多次给药的I期临床试验(N=46),旨在评价维莫非尼在BRAFV600突变阳性的不能切除或转移性黑色素瘤中国患者中的药代动力学、安全性和疗效。研究的主要终点为药代动力学指标,次要终点包括:经确认的BORR、缓解持续时间、PFS、OS和安全性。
患者中位年龄为42岁,其中4.3%的患者年龄大于65岁。大多数患者为女性(54%),疾病分期为M1c(61%)。所有患者的ECOG体能状态为0或1分。67%的患者既往至少接受过一次针对转移性黑色素瘤的系统性治疗。中位随访时间为11.3个月(范围3.3至16.0个月之间)。
疗效性结果
由研究者评估,经确认的最佳总体缓解率(CR+PR)为52%(95%置信区间:37%,67%)。中位至疾病缓解时间为1.8个月。缓解持续时间的中位值为9.1个月(95%置信区间:7.4,未达到)。在46%的患者中,观察到基于RECIST1.1判定的疾病稳定。中位PFS为8.3个月(95%置信区间:5.7,10.9),6个月PFS率为59%(95%置信区间:45%,73%),12个月PFS率为33%(95%置信区间:20%,47%)。中位总生存期为13.5个月(95%置信区间:12.2个月,未达到),6个月生存率为89%(95%置信区间:80%,98%),12个月生存率为65%(95%置信区间:51%,79%)。
安全性结果
最新的安全性分析是基于临床研究报告更新的安全分析人群(N=46)进行的(数据截止日期为2014年12月15日)。总体而言,维莫非尼的耐受性良好。
最常见的AE为痤疮样皮炎和关节痛(各30例患者,65.2%),其次是血胆固醇升高和腹泻(各27例患者,58.7%)、血胆红素升高(25例患者,54.3%)、黑色素痣(24例患者,52.2%)、脱发(23例患者,50.0%)、掌跖红肿疼痛综合征(22例患者,47.8%)、光敏反应(17例患者,37.0%)、疲劳(14例患者,30.4%)、发热(13例患者,28.3%)、斑丘疹(12例患者,26.1%)、γ-谷氨酰转移酶升高和蛋白尿(各11例患者,23.9%)以及总胆酸升高、高甘油三酯血症和白细胞减少(各10例患者,21.7%)。
遗传毒性:在Ames试验、人淋巴细胞染色体畸变试验、大鼠骨髓微核试验中,未显示维莫非尼具有遗传毒性。
生殖毒性:尚未进行维莫非尼对动物生育力影响的专项研究。重复给药毒性试验中,大鼠和犬的剂量达到450mg/kg/日时,以AUC计,雌、雄大鼠的暴露量分别为人临床暴露量的1.6和0.6倍,犬的暴露量为人临床暴露量的0.4倍,均未观察到动物的生殖器官出现组织病理学变化。维莫非尼在250mg/kg/日(以AUC计,大鼠的暴露量相当于人临床暴露量的1.7倍)时,在450mg/kg/日(以AUC计,家兔的暴露量相当于人临床暴露量的0.7倍)时,对大鼠和家兔胚胎/胎仔的发育未见致畸作用。胎仔的药物水平是母体水平的3~5%,提示维莫非尼可以从母体中转运进入发育的胎仔体内。
致癌性:尚未进行维莫非尼的致癌性研究。维莫非尼可引起植入人cuSCC细胞的移植瘤小鼠的肿瘤生长呈剂量依赖性增加。临床试验中,维莫非尼可增加患者皮肤鳞状细胞癌的发生率。