肝脏毒性 在临床研究中发生了严重的、有时是致命性的肝脏毒性; 在治疗前及治疗中进行肝功能监测; 在使用瑞戈非尼片治疗中,可根据肝功检测或肝细胞坏死所表现出来的肝脏毒性的严重程度和持续性,暂停后降低剂量或停药。
- 药品名称:
- 通用名称:瑞戈非尼片
英文名称:Stivarga(Regorafenib Tablets)
商品名称:拜万戈
- 成份:
主要成份:瑞戈非尼
化学名称:4-[4-({[4-氯-3-(三氟甲基)苯基]氨基甲酰}氨基)-3-氟苯氧基]-N-甲基吡啶-2-甲酰胺一水合物
化学结构式:
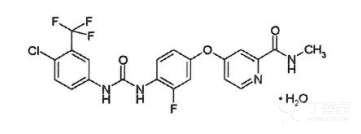
分子式:C21H15CLF4N4O3·H2O
分子量:500.83
- 适应症:
适用于治疗既往接受过以氟尿嘧啶、奥沙利铂和伊立替康为基础的化疗,以及既往接受过或不适合接受抗VEGF治疗、抗EGFR治疗(RAS野生型)的转移性结直肠癌(mCRC)患者。
既往接受过甲磺酸伊马替尼及苹果酸舒尼替尼治疗的局部晚期的、无法手术切除的或转移性的胃肠道间质瘤(GIST)患者。
既往接受过索拉非尼治疗的肝细胞癌(HCC)患者。
- 用法用量:
瑞戈非尼应由在抗癌治疗给药方面有经验的医生开具。
推荐剂量
推荐剂量为160mg(4片,每片含40mg瑞戈非尼),每日一次,于每一疗程的前21天口服,28天为一疗程。
服用方法
瑞戈非尼片应在每天同一时间,在低脂早餐(脂肪含量30%)后随水整片吞服。患者不得在同一天服用两剂药物以弥补(前一天)漏服的剂量。如果服用瑞戈非尼后出现呕吐,同一天内患者不得再次服药。
治疗时间
应持续治疗直至患者不能临床受益或出现不可耐受的毒性反应。
剂量调整及特殊使用说明
基于个人的安全性及耐受性考虑,可能需要中断给药或降低剂量。应采用每次40mg(一片)的剂量调整。建议每日最低剂量为80mg。每日最高剂量为160mg。
发生手足皮肤反应[HFSR/PPE(掌跖红肿疼痛综合征)]时的剂量调整及措施请参见表1。
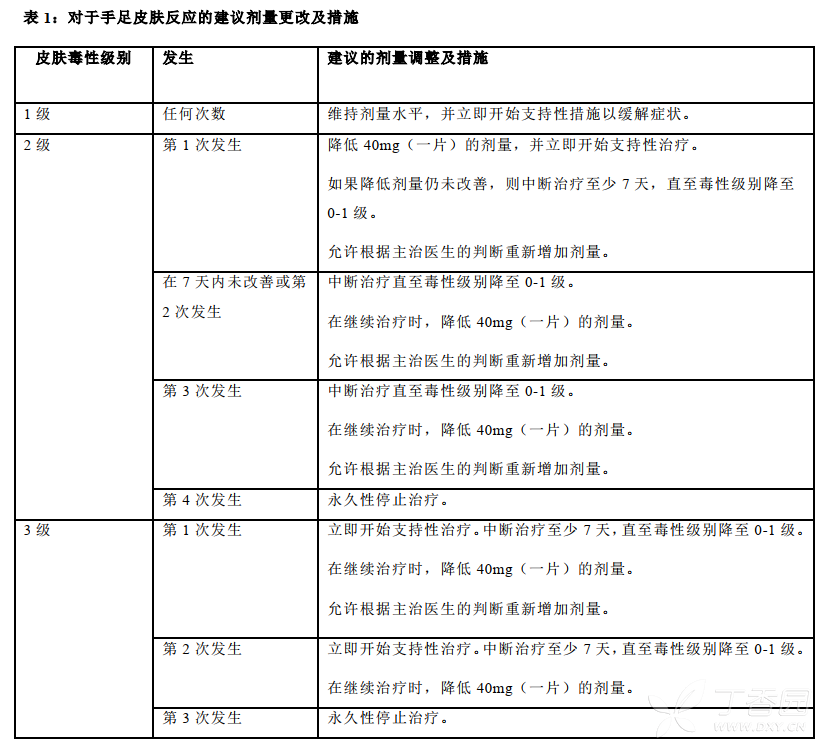
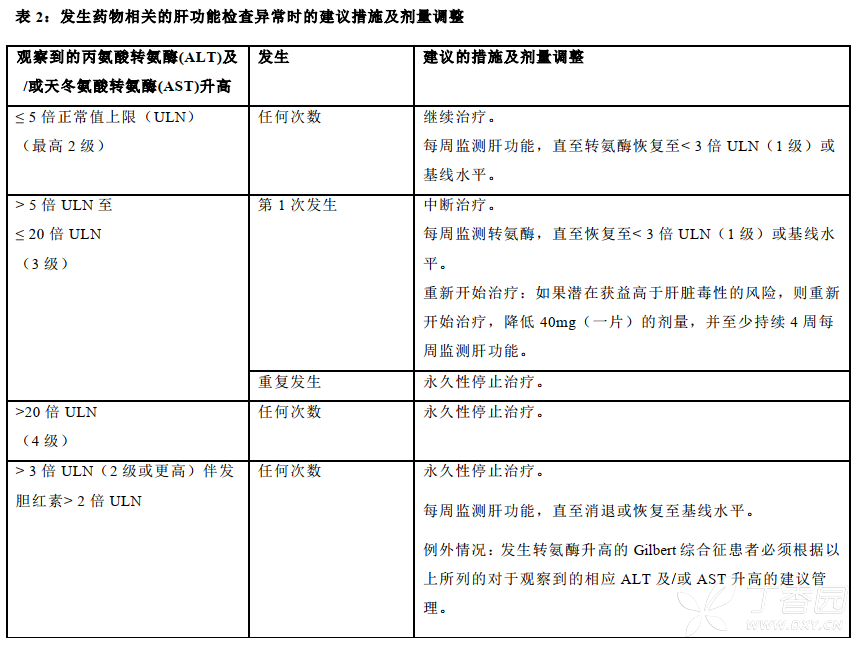
如果肝功能检查结果恶化并认为与瑞戈非尼治疗有关,建议的措施和剂量调整见表2(同时请参见“注意事项”)。
特殊人群
肝损伤患者
在临床研究中,肝功能Child-Pugh A患者不必调整剂量。由于肝功能Child-Pugh B患者数据有限,因此不能提供剂量调整建议。建议对此类患者严密监测总体安全性(见“注意事项”)。
由于尚未对瑞戈非尼治疗肝功能Child-Pugh C患者进行研究,因此不建议瑞戈非尼用于此类人群。
肾损伤患者
现有临床数据表明,轻度、中度或重度肾损伤患者与肾功能正常患者相比,瑞戈非尼及其代谢产物M-2和M-5的暴
露量相似。轻度、中度或重度肾损伤患者不必调整剂量。见“药代动力学”肾损伤。)
性别
在临床研究中,男性患者与女性患者间在暴露量、安全性或有效性方面无相关差异。无需根据性别调整剂量。
种族差异
在临床研究中,不同种族患者在暴露量或有效性方面无相关差异,无需根据种族调整剂量。
- 不良反应:
- 1. 安全性特征总结: 瑞戈非尼的总体安全性特征基于来自1200多名在临床研究中接受治疗的患者的数据,包括500名转移性结直肠癌(mCRC)患者以及132名胃肠道间质瘤(GIST)患者的安慰剂对照Ⅲ期...
- 禁忌:
- 对活性物质或辅料有超敏反应的患者。
- 注意事项:
肝脏毒性
肝功能检查(ALT、AST及胆红素)异常常见于瑞戈非尼治疗组患者。少部分患者中报告了重度肝功能检查异常(3至4级)和伴有临床表现(包括致命结局)的肝功能障碍(见“不良反应”)。与高加索人相比,在临床研究中接受瑞戈非尼治疗的亚洲(尤其是日本)患者重度肝功能检查异常以及肝功能障碍的发生率较高。
建议在开始瑞戈非尼治疗之前进行肝功能检查(ALT、AST及胆红素),并在治疗开始的2月内严密监测(至少两周一次)。此后,应至少每月定期监测或有临床指征时监测。
瑞戈非尼是一种尿苷二磷酸葡萄糖醛酸转移酶(UGT)1A1抑制剂(见“药物相互作用”)。Gilbert综合征患者可能出现轻度间接(未结合)高胆红素血症。
观察到肝功能检查恶化且认为与瑞戈非尼治疗有关的患者(即没有明显的其他原因,如肝后胆汁淤积或疾病进展),应采取表2中的剂量改变和监测建议。
瑞戈非尼主要经肝脏途径消除。建议对轻度或中度肝损伤患者严密监测总体安全性(见“用法用量”和“药代动力学”)。由于尚未对瑞戈非尼治疗肝功能Child-Pugh C患者进行研究,并且此类患者体内暴露量可能增加,因此不建议瑞戈非尼用于此类人群。
感染
研究表明,瑞戈非尼与感染事件发生率升高相关,其中一些事件是致命的(见“不良反应”)。
在出现感染恶化的情况下,应考虑中断瑞戈非尼治疗。
出血
研究表明,瑞戈非尼与出血事件发生率升高相关,其中一些事件是致命的(见“不良反应”)。对患诱发出血疾病的患者,使用抗凝药(如华法林和苯并羟基香豆素)或其他由于伴随用药增加出血风险的患者,应监测血细胞计数和凝血参数。开始瑞戈非尼治疗前,肝硬化患者的食管静脉曲张筛查和后续治疗应根据标准治疗实践进行。如果出现需要紧急医学干预的重度出血,应考虑永久停用瑞戈非尼。
胃肠道穿孔及瘘管
瑞戈非尼治疗的患者报告出现胃肠道穿孔(包括致命结局)和瘘(见“不良反应”)。这些事件也是腹腔内恶性肿
瘤患者常见的与疾病有关的并发症。建议对出现胃肠道穿孔或瘘的患者停用瑞戈非尼。
心肌缺血及梗死
研究表明,瑞戈非尼与心肌缺血和心肌梗死发生率升高相关(见“不良反应”)。不稳定型心绞痛或新发心绞痛(开始瑞戈
非尼治疗之前3个月内)、近期心肌梗死(开始瑞戈非尼治疗之前6个月内)的患者和纽约心脏病协会(NYHA)2级或以上的心力衰竭患者均未被纳入临床研究。
有缺血性心脏病史的患者应监测心肌缺血的临床体征和症状。对于出现心肌缺血和(或)梗死的患者,建议中断瑞戈非尼直至恢复。对个例患者潜在获益和风险进行仔细考虑后,可做出重新开始瑞戈非尼治疗的决定。如果未恢复,应永久停用瑞戈非尼。
可逆性后部脑病综合征(PRES)
据报告PRES与瑞戈非尼治疗相关(见“不良反应”)。PRES的体征和症状包括癫痫发作、头痛、精神状态改变、
视力障碍或皮质盲,伴随或不伴随有高血压。PRES的诊断需要脑成像证实。对于患PRES的患者,建议停用瑞戈非尼,并控制高血压,对其他症状采取支持性医学管理。
动脉高血压
研究表明,瑞戈非尼可导致动脉高血压发生率升高(见“不良反应”)。开始瑞戈非尼治疗之前应控制血压。建议监测血压并依照标准医疗实践处置高血压。如果尽管采取足够的医学管理仍出现重度或持久性高血压,经临床医生同意,应暂时中断治疗和(或)减少剂量。如果出现高血压危象,应终止瑞戈非尼治疗。
皮肤毒性
手足皮肤反应(HFSR)或掌跖红肿疼痛综合征和皮疹是瑞戈非尼治疗时最常见的皮肤不良反应(见“不良反应”)。
与高加索人比,在临床研究中接受瑞戈非尼治疗的亚洲(尤其是日本)患者HFSR的发生率更高。预防HFSR的措施包括控制胼胝,使用鞋垫和手套,防止对足底和手掌的压迫。HFSR的管理可能包括使用角质层分离剂乳剂(如含尿素、水杨酸或α羟基酸的乳剂,仅局部涂覆于受累区域)和保湿霜(随意涂覆)缓解症状。如果出现不良反应,应考虑减少剂量或暂时中断瑞戈非尼,如果不良反应是重度或持续性的,应考虑永久停用瑞戈非尼(见“用法用量”)。
生化及代谢实验室检查异常
研究表明,瑞戈非尼与电解质异常(包括低磷酸血症、低钙血症、低钠血症及低钾血症)及代谢异常(包括促甲状腺激素、脂肪酶及淀粉酶升高)的发生率升高有关。这些异常一般为轻度至中度,并无临床表现,且通常不需要中断给药或降低剂量。建议在瑞戈非尼治疗期间监测生化及代谢参数,并在需要时根据标准临床实践开始适当的替代疗法。如果出现持续或反复的显著异常,应考虑中断给药或降低剂量,或永久性停止瑞戈非尼治疗。
伤口愈合并发症
由于具有抗血管生成性质的药品可能抑制或妨碍伤口愈合,为预防起见,建议对接受大手术的患者暂时中断瑞戈
非尼。在大手术后,只有经临床判断伤口愈合充分,可做出恢复瑞戈非尼治疗的决定。
关于辅料的重要信息
每160 mg的日剂量含2.427 mmol(或55.8 mg)的钠。患者应考虑在饮食中控制钠的摄入量。每个160 mg的日剂量含1.68mg的卵磷脂(来源于大豆)。
对驾驶和使用机器能力的影响
没有关于瑞戈非尼对驾驶或使用机器的能力影响的研究。如果患者在瑞戈非尼治疗期间出现影响其注意力和反应的症状,
建议其在影响消除后再驾驶或使用机器。
疾病特异性注意事项-肝细胞癌(HCC)
在关键性安慰剂对照III期研究中,患者既往接受过索拉非尼治疗。因索拉非尼相关毒性或仅耐受低剂量(每日<400 mg)而中止索拉非尼治疗的患者的数据不足。尚未确定瑞戈非尼在这些患者中的耐受性。
- 药物相互作用:
CYP3A4和UGT1A9的抑制剂或CYP3A4的诱导剂
体外数据表明,瑞戈非尼由细胞色素CYP3A4和尿苷二磷酸葡萄糖醛酸转移酶UGT1A9代谢。
酮康唑是一种强CYP3A4抑制剂,该药(400 mg,给药18天)联合单剂量瑞戈非尼(160 mg,第5天给药)给药,导致瑞戈非尼的平均暴露量(AUC)增加约33%,活性代谢产物M-2(氮氧化物)和M5(氮氧化物和N-去甲基)的平均暴露量减少约90%。由于尚未研究CYP3A4活性的强抑制剂(如克林霉素、葡萄柚汁、伊曲康唑、酮康唑、泊沙康唑、泰利霉素和伏立康唑)对瑞戈非尼及其代谢产物的稳态暴露量的影响,建议避免同时使用这些药物。
由于尚未研究强UGT1A9抑制剂(如甲灭酸、二氟尼柳和尼氟酸)对瑞戈非尼及其代谢产物的稳态暴露量的影响,建议瑞戈非尼治疗期间应避免同时给药。
利福平是一种强CYP3A4诱导剂,该药(600 mg,给药9天)联合单剂量瑞戈非尼(160 mg,第7天给药)给药,导致瑞戈非尼的AUC减少约50%,活性代谢产物M-5的平均暴露量增加3至4倍,活性代谢产物M-2的暴露量没有变化。其他强CYP3A4诱导剂(如苯妥英、卡马西平、苯巴比妥和贯叶连翘)可能也促进瑞戈非尼的代谢。应避免同时服用强CYP3A4诱导剂,或者应考虑选择无诱导CYP3A4可能性或诱导可能性极小的替代合并用药。
UGT1A1和UGT1A9底物
体外数据表明,瑞戈非尼及其活性代谢产物M-2抑制UGT1A1和UGT1A9介导的葡萄糖醛酸苷化,而M-5仅在体内达到稳态时的浓度下才抑制UGT1A1。瑞戈非尼给药中断5天后给予伊立替康,导致SN-38(一种UGT1A1的底物和伊立替康的活性代谢产物)的AUC增加约44%。同时,也观察到伊立替康的AUC增加约28%。这表明联合使用瑞戈非尼可能增加UGT1A1和UGT1A9底物的全身暴露量。
乳腺癌耐药蛋白(BCRP)和P-糖蛋白底物
瑞舒伐他汀(5 mg)(BCRP的一种底物)单次给药前给予瑞戈非尼(160 mg,共14日),可导致瑞舒伐他汀的暴露量(AUC)均值升高3.8倍,Cmax升高4.6倍。 此结果表明,瑞戈非尼合并用药可能会增加其他BCRP底物合并用药(如甲氨蝶呤、氟伐他汀及阿托伐他汀)的血浆浓度。因此,建议密切监测患者因BCRP底物暴露量增加而出现的相关体征及症状。
临床数据表明,瑞戈非尼对于地高辛的药代动力学性质没有影响,因此本品可与地高辛等P-糖蛋白底物合并用药,不会出现具有临床意义的药物相互作用。
P-糖蛋白和BCRP的抑制剂或P-糖蛋白的诱导剂
体外研究表明活性代谢产物M-2和M-5是P-糖蛋白和BCRP的底物。BCRP和P-糖蛋白的抑制剂和诱导剂可能妨碍M-2和M-5的暴露。这些发现的临床意义不明。
CYP亚型选择性底物
体外数据表明,在体内达到稳态(峰浓度8.1微摩尔)的浓度下,瑞戈非尼是细胞色素CYP2C8(Ki值0.6微摩尔)、CYP2C9(Ki值4.7微摩尔)、CYP2B6(Ki值5.2微摩尔)的竞争性抑制剂。对CYP3A4(Ki值11.1微摩尔)和CYP2C19(Ki值16.4微摩尔)的体外抑制效力不太显著。
为评价瑞戈非尼160 mg给药14天对CYP2C8(罗格列酮)、CYP2C9(S型华法林)、CYP 2C19(奥美拉唑)和CYP3A4(咪达唑仑)的探针底物的药代动力学影响,实施了一项探针底物临床研究。
药代动力学数据表明,瑞戈非尼可以与CYP2C8、CYP2C9、CYP3A4和CYP2C19底物同时给药,而不会发生有临床意义的药物相互作用(见“注意事项”)。
抗生素
浓度时间曲线显示,瑞戈非尼及其代谢产物可能经历肝肠循环(见“药代动力学”)。在与新霉素联合使用的情况下,由于新霉素是一种体内吸收较差、用于根除胃肠微生物菌群的抗菌药物(可能会干扰瑞戈非尼的肝肠循环),尽管瑞戈非尼的暴露量没有受到影响,但是与瑞戈非尼具有类似体内外药理作用的活性代谢产物M-2及M-5的暴露量则下降了约80%。与新霉素这种相互作用的临床意义仍有待阐明,但是可能会降低瑞戈非尼的有效性。目前尚未对其他抗生素在药代动力学方面的相互作用进行研究。
胆盐螯合剂
瑞戈非尼、M-2和M-5可能经历肝肠循环。考来烯胺和考来胶等胆盐螯合剂可能通过形成不溶性复合物与瑞戈非尼发生相互作用,这种复合物可能影响吸收(或再吸收),从而可能导致暴露量减少。这些潜在相互作用的临床意义不明,但可能导致瑞戈非尼有效性降低。
- 临床试验:
转移性结直肠癌(mCRC)
在标准治疗失败后疾病进展的760例转移性结直肠癌患者中进行的一项国际、多中心、随机(2:1)、双盲、安慰剂对照Ⅲ期研究( CORRECT)中,评估了瑞戈非尼的临床有效性及安全性。
主要有效性终点为总生存期(0s)。次要终点为无进展生存期(PFS)、客观肿瘤应答率和疾病 控制率。
患者随机口服160mg的瑞戈非尼,每日一次加最佳支持治疗(N=505),或匹配安慰剂加最佳支持治疗(N=255),28天为一疗程,每一疗程的前21天予以治疗。患者持续治疗直至疾病进展或出现不可接受的毒性。
在760例随机化的患者中,中位年龄61岁,61%为男性,78%为高加索人,所有患者ECOG基线体力状态为0或1分。在瑞戈非尼治疗期间11.4%的患者报告PS≥2。中位治疗时间和日剂量以及剂量改变和剂量减少率与接受安慰剂PS≥2的患者(8.3%)的报告相似。大多数PS≥2的患者因疾病进展停止治疗。
疾病的原发部位为结肠(65%)、盲肠(29%)或两者皆有(6%)。多数患者(52%)因转移性疾病接受过3线或更少线的治疗。治疗包括氟嘧啶化疗治疗、一种抗VEGF治疗和一种抗EGFR治疗(如果患者为KRAS野生型)。
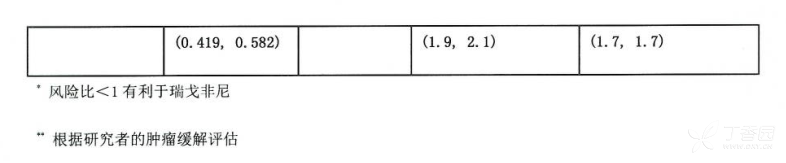
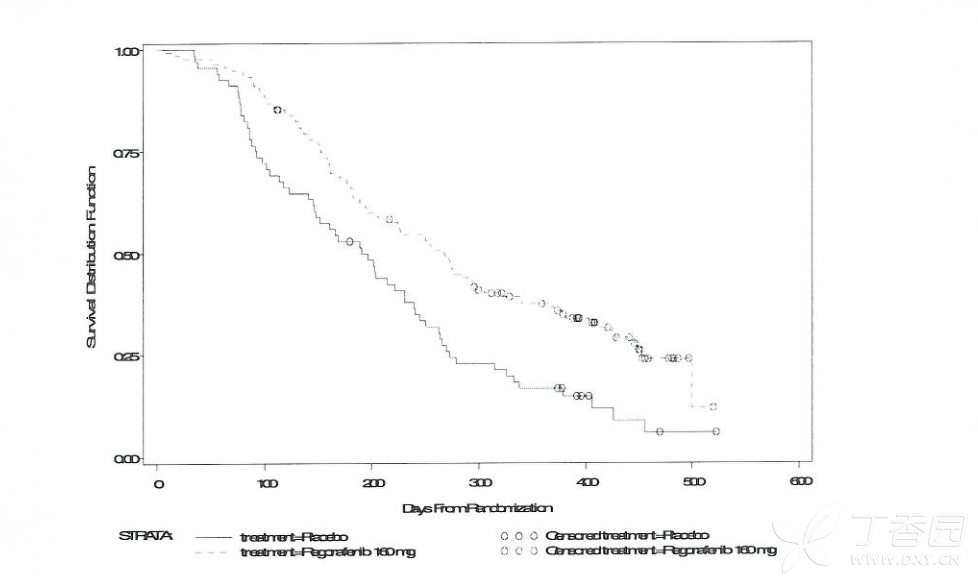
瑞戈非尼加最佳支持治疗对比安慰剂加最佳支持治疗的总生存期显著延长,风险比0.774(p=0.005178,分层对数秩检验),中位0s分别为6.4个月和5.0个月【95% CI 0.636,0.942】(见表6和图1)。接受瑞戈非尼加最佳支持治疗治疗的患者PFS显著增长(风险比:0.494,p<0.00000,见表6)。瑞戈非尼和安慰剂治疗的患者缓解率(完全缓解或部分缓解)分别为1%和0.4%(p=0.188432单侧)。瑞戈非尼治疗的患者疾病控制率(完全缓解或部分缓解或疾病稳定)显著提高(41.0%149%,p<0.00001,单侧)。
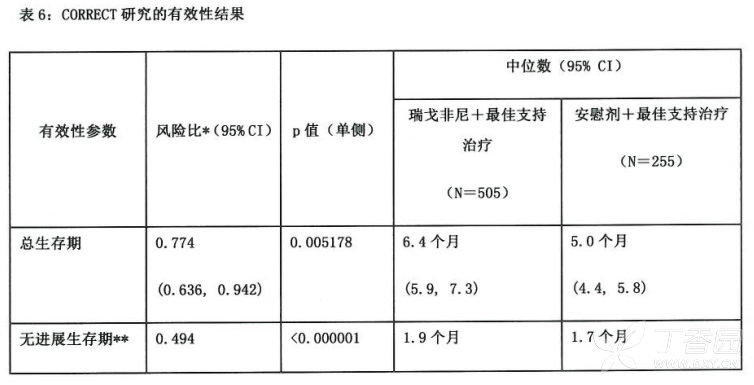
另一项Ⅲ期、国际、多中心、随机化、双盲、安慰剂对照研究( CONCUR)在204例以前接受氟嘧啶化疗失败后出现进展的转移性结直肠癌亚洲患者(84.3%为中国患者)中评价瑞戈非尼的有效性和安全性。
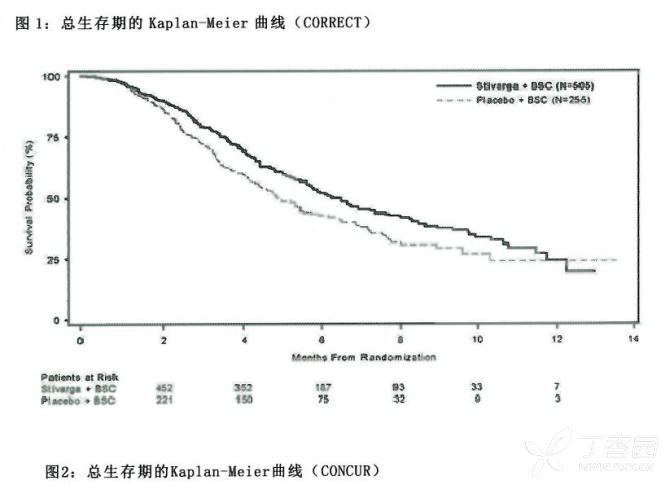
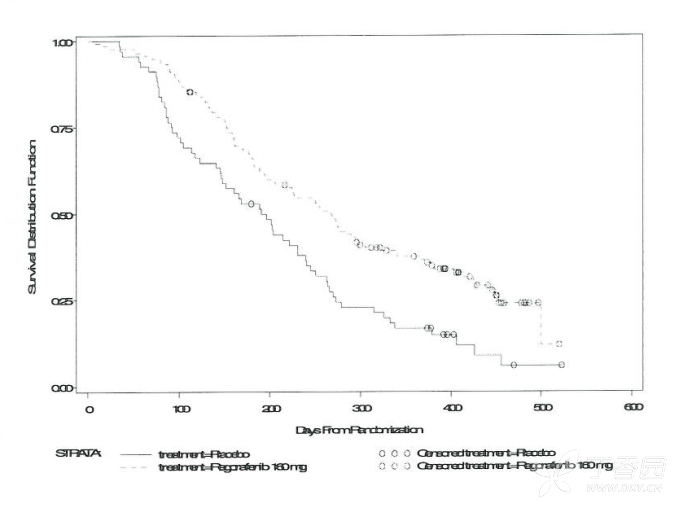
CONCUR研究中,59.5%的患者以前曾接受过VEGF和/或EGFR靶向药物治疗。主要有效性终点是0。与安慰剂加最佳支持治疗相比,瑞戈非尼加最佳支持治疗的生存期显著延长,风险比0.550(p=0.000159分层对数秩检验),中位0S分别为88个月和6.3个月【95%CI 0.395,0.765】。接受瑞戈非尼加最佳支持治疗的患者的PFS显著延长(风险比:0.311,p<0.0000),瑞戈非尼组和安慰剂组的中位PFS分别为3.2个月和1.7个月。
CONCUR研究中,瑞戈非尼加最佳支持治疗的安全性特征与 CORRECT研究中观察到的安全性特征一致。在中国患者中未观察到新的、非预期的安全性问题。
胃肠道间质瘤(GIST)
在一项国际、多中心、随机化、双盲、安慰剂对照III期研究(GRID)中评价了瑞戈非尼的临床有效性和安全性,研究对象是经2种酪氨酸激酶抑制剂(伊马替尼和舒尼替尼)既往治疗过的胃肠道间质瘤(GIST)患者。
在144例PFS事件后进行了主要有效性终点无进展生存期的分析(中心设盲评估)。也评估了次要终点,包括进展时间(TTP)和总生存期(0S)(中期分析)。
共199例GIST患者以2:1的比例随机接受160mg瑞戈非尼加最佳支持治疗(N=133)口服一天一次或匹配安慰剂加最佳支持治疗(N=66)治疗3周,然后停止治疗1周。接受瑞戈非尼的平均日剂量为140mg。
患者持续治疗,直至疾病进展或出现不可接受的毒性。向出现疾病进展的接受安慰剂的患者提供开放性的瑞戈非尼治疗(交叉选择)。接受瑞戈非尼的患者如果出现疾病进展并且研究者认为患者接受瑞戈非尼治疗仍然有临床获益,则提供继续服用开放性的瑞戈非尼的机会。
在199例随机化的患者中,平均年龄58岁,64%为男性,68%为白种人,所有患者ECOG基线体力状态为0或1分。从最近进展或复发至随机化的总中位时间为6周。
瑞戈非尼加最佳支持治疗的PFS比安慰剂加最佳支持治疗要显著延长,风险比0.268[95%CI 0.185,0.388],中位PFS分别为4.8个月和0.9个月(p<0.000001)。瑞戈非尼治疗的患者疾病进展或死亡的相对风险比安慰剂治疗的患者下降约73.2%(见表7、图3)。PFS延长具有一致性,与年龄、性别、地区、既往治疗线数、ECOG、PS无关。
瑞戈非尼加最佳支持治疗导致TTP显著长于安慰剂加最佳支持治疗,风险比0.248[95%CI 0.170,0.364],中位TTP分别为5.4个月和0.9个月(p<0.000001)(见表7)。
0S的HR为0.772(95%CI,0.423,1.408;p=0.199;两组均未达到中位0S):85%的初始随机至安慰剂组的患者接受进展后瑞戈非尼治疗(见表7)。

图3:无进展生存期的Kaplan-Meier 曲线

此外,56例安慰剂加最佳支持治疗患者在疾病进展后接受开放性的瑞戈非尼治疗,41例瑞戈非尼加最佳支持治疗患者疾病进展后继续瑞戈非尼治疗。中位PPS(由研究者评估测量)分别为5.0和4.5个月。
- 毒理研究:
一般毒性:
在大鼠26周重复给药毒性试验中可见剂量依赖性房室瓣增厚,瑞戈非尼在相当于人临床推荐剂量时暴露量12%的剂量下,50%的动物出现房室瓣增厚。
大鼠28天重复给药毒性试验显示,瑞戈非尼4mg/kg时(按AUC计算约为人临床推荐剂量的25%)可见牙质改变及血管扩张。犬13周重复给药毒性试验中,瑞戈非尼20mg/kg时(按AUC计算约为人临床推荐剂量的43%)可见相似的牙质改变。瑞戈非尼可引起动物股骨垢生长板持续生长并增厚。幼龄动物给药后可见更明显的牙齿、骨骼、生殖系统的毒性反应,提示瑞戈非尼对儿童和青少年有潜在的安全风险。
遗传毒性:
瑞戈非尼体外和体内遗传毒性试验结果阴性,瑞戈非尼人体主要代谢产物M-2中国仓鼠V9细胞染色体畸变试验结果阳性。
生殖毒性:
瑞戈非尼在低于人预期暴露量(临床推荐剂量时)时,引起大鼠、兔的胚胎死亡,并有致畸作用,如泌尿系统、心脏与大血管、骨骼的畸形发生率增加。妊娠大鼠单次给药的分布试验中,瑞戈非尼胎仔血脑屏障通过率高于母体。胚胎-胎仔发育毒性试验中,大鼠中瑞戈非尼1mg/kg(按体表面积计算约为人临床推荐剂量的6%)可见胚胎完全丢失(100%重吸收),兔中1.6mg/kg(按AUC计算约为人临床推荐剂量的25%)可见胚胎完全丢失(100%重吸收)。
妊娠大鼠器官形成期给予瑞戈非尼,≥0.8mg/kg组(按体表面积计算约为人临床推荐剂量的5%)可见胎仔骨化延迟及骨骼畸形(如腭裂),发生率呈剂量依赖性增加;≥1mg/kg组(按AUC计算约为人临床推荐剂量的10%),胎仔的囟门变大;≥1.6mg/kg组(按体表面积计算约为人临床推荐剂量的5%)胎仔心血管畸形、外观异常、膈疝、肾盂扩张的发生率呈剂量依赖性增加。
妊娠兔器官形成期给予瑞戈非尼,最低剂量0.4mg/kg组(按AUC计算约为人临床推荐剂量的7%)可见室中隔缺陷,≥0.8mg/kg组(按AUC计算约人临床推荐剂量的15%)可见心血管畸形、骨骼异常发生率增加,并可见泌尿系统异常如肾脏/输尿管缺失,肾脏偏小、畸形及位置异常,肾盂积水。两项兔胚胎-胎仔发育毒性试验中,成活胎仔中雄性动物的比例随剂量增加而降低。
尚未进行瑞戈非尼生育力影响试验。瑞戈非尼在与人临床推荐剂量下有相似暴露量(AUC)的剂量时,可见雄性大鼠肾小管萎缩、睾丸退化、精囊萎缩、附睾出现细胞碎片、精子减少,雌性大鼠黄体坏死增加。犬重复给药试验中,瑞戈非尼在相当于人临床推荐剂量时暴露量(AUC)的83%剂量时,雌雄犬出现与大鼠相似的变化。
致癌性
尚未进行瑞戈非尼致癌性试验
瑞格菲尼资料来源