孟加拉 Osimertinib Osicent 80mg ( Incepta )奥希替尼 奧西替尼 白盒9291 泰瑞沙 奥西替尼
非小细胞肺癌(NSCLC),
| 数量: | 库存 104827 件 |
产品名称 : 吉泰瑞
通用名称 : 奥希替尼 (白盒9291)
剂型 : 片剂
包装 : 30 片
规格 : 80 mg
产地 : 孟加拉国 Incepta
【适应症】
处方药。非小细胞肺癌:有转移的非小细胞肺癌,使用壹代EGFR TKI靶向药耐药的,有表皮生长因子受体EGFR T790M突变的患者。
【作用机制】
奥希替尼Osimertinib是壹个EGFR酪氨酸激酶抑制剂,不可逆的与特定的EGFR突变结合,包括T790M,L858R和19号外显子缺失等。奥希替尼(AZD9291)被选择性的用于敏感性突变和T790M耐药突变(该突变为壹代EGFR TKI类靶向药最常见的耐药因素)
【副作用】
腹泻,皮疹,皮肤干燥,恶心,眼病,食欲减退,便秘等;严重的副作用如肺炎、肺栓塞等。
AZ 9 2 91(泰瑞 沙、奥 希 替尼)是凯美纳、易 瑞 沙和特 罗 凯 耐药后的治疗晚期肺癌的口服靶向药。曾服用易 瑞 沙、特 罗凯、及国产凯美纳的晚期肺癌患者,平均6-12月就产生耐药了,耐药以后壹般会有50%-60%的患者T790M突变,而这类患者就非常适合服用泰瑞沙。
剂量:
泰 瑞 沙壹般是20-80mg,1天1次,空腹或者随餐服药都可以。推荐剂量是80mg,每日1次(直至出现疾病进展或无法耐受的毒性作用)。如果有壹次忘记吃了,那么12小时之内应该加上那次忘记吃的药。
如果副作用太大,那么可以减量到40mg,1天1次。
脑转移患者也是80mg,如果是脑膜转移,那么剂量要加倍,也就是160mg,1天1次。
不良反应方面,Tagrisso(A Z 9 2 91)和传统的靶向药物(易 瑞 沙 特 罗凯等)较壹致,副反应不大。最常见的主要是腹泻、皮疹、皮肤干燥、指甲毒性、消化道反应等。
壹般程度比较轻,对症处理就能缓解。除此,少数的患者(不足10%)可能会出现间质性肺炎、QT间期延长、心肌炎等较为严重的不良反应,发生概率很低。
如在用药时出现相应症状请及时复查随诊,与主治医师保持沟通。每个患者是否出现不良反应是存在个体差异的.
百度百科您身边的百科全书
本品活性成份为甲磺酸奥希替尼
化学名称:N-{2-{2-(二甲氨基)乙基氨基}-4-甲氧基-5-{[4-(l-甲基-lH-吲哚-3-基)嘧啶-2-基]氨基}苯基)丙-2烯酰胺甲磺酸盐
化学结构式:

分子式: C28H33N7O2 . CH4O3S
分子量: 595.71
本品应由在抗肿瘤治疗方面富有经验的医生处方使用。
在使用本品治疗局部晚期或转移性NSCLC前,首先需要明确EGFRT790M突变的状态。应采用经过充分验证的检测方法确定存在EGFRT790M突变方可使用本品治疗(详见【注意事项】)。
剂量
本品的推荐剂量为每日80mg,直至疾病进展或出现无法耐受的毒性。
如果漏服本品1次,则应补服本品,除非下次服药时间在12小时以内。
本品应在每日相同的时间服用,进餐或空腹时服用均可。
剂量调整
根据患者个体的安全性和耐受性,可暂停用药或减量。如果需要减量,则剂量应减至40mg,每日1次。
出现不良事件(AE)和毒性后的减量原则请见表1。

特殊人群
无需因为患者的年龄、体重、性别、种族和吸烟状态对剂量进行调整(见【药代动力学】)。
肝功能损害
轻度肝功能损害(总胆红素<正常值上限(ULN)且谷草转氨酶(AST)达1至1.5xULN;或总胆红素达1至1.5xULN,AST不限)患者无需进行剂量调整,但此类患者仍应慎用本品。中重度肝功能损害患者使用本品的安全性和有效性尚不明确。在获得更多信息前,不建议中重度肝功能损害患者使用本品。(见【药代动力学】)。
肾功能损害
轻中度肾功能损害患者使用本品时无需进行剂量调整。重度肾功能损害患者使用本品的数据有限。终末期肾病(经Cockcroft和Gault方程计算的肌酐清除率(CLcr)<15mL/min)或正在接受透析的患者使用本品的安全性和有效性尚不明确。患有重度或终末期肾功能损害的患者应慎用本品(见【药代动力学】)。
给药方法
本品为口服使用。本品应整片和水送服,不应压碎、掰断或咀嚼。
如果患者无法吞咽药物,则可将药片溶于50mL不含碳酸盐的水中。应将药片投入水中,无需压碎,直接搅拌至分散后迅速吞服。随后应再加入半杯水,以保证杯内无残留,随后迅速饮用。不应添加其它液体。
需要经胃管喂饲时,可采用和上述相同的方式进行处理,只是最初溶解药物时用水15mL,后续残余物冲洗时用水15mL。这30mL液体均应按鼻胃管生产商的说明进行喂饲,同时用适量的水冲洗。这些溶解液和残余液均应在将药片加入水中后30分钟内服用。
安全性数据总结(不考虑因果关系)
在两项全球单臂临床试验中(AURA扩展研究II期部分和AURA2研究)获得了411名既往接受过治疗的T790M突变阳性的NSCLC患者使用本品的安全性数据,这些患者服用的剂量为每日80mg。411例患者中,333例暴露于本品治疗至少6个月;97例患者暴露至少9个月;但是,无患者暴露达12个月。
本品治疗组患者中最常见(>20%)不良事件为腹泻(42%)、皮疹(41%)、皮肤干燥(31%)和指(趾)甲毒性(25%)。
导致剂量减少或中断治疗的最常见不良事件为心电图QTc间期延长(2.2%)和中性粒细胞减少(1.9%)。2%或2%以上患者报告的严重不良事件为肺炎和肺栓塞。本品治疗组4例患者(1%)出现致死性间质性肺病/非感染性肺炎不良事件。
1例以上患者报告的其它致死性不良事件包括感染性肺炎(4例患者)和心脑血管意外/脑出血(2例患者)。本品治疗组5.6%患者因不良事件而中止治疗。导致中止治疗的最常见不良事件为间质性肺病/非感染性肺炎和脑血管意外/脑梗死。


安全性数据总结(明确为药物不良反应的部分)
表3列举了服用本品的患者中常见的药物不良反应(ADR)发生率。
不良反应根据MedDRA的系统器官分类(SOC)进行列表。在每个系统器官分类内部按发生频率对ADR进行了排列,其中频率最高的ADR居首。在每个频率类别内则按严重程度的降序对ADR进行排列。
此外,依据CIOMSIII的常规概念对每项ADR相应的发生频率进行了归类,这些发生频率的类别为:极常见(≥1/10);常见(>1/100至<1/10);少见(≥1/1,000至<1/100);罕见(≥1/10,000至<1/1,000);极罕见(<1/10,000);不详(根据现有数据无法估计)。本节仅纳入了已经结束的研究获得的数据,在这些研究中,患者的暴露量是已知的。

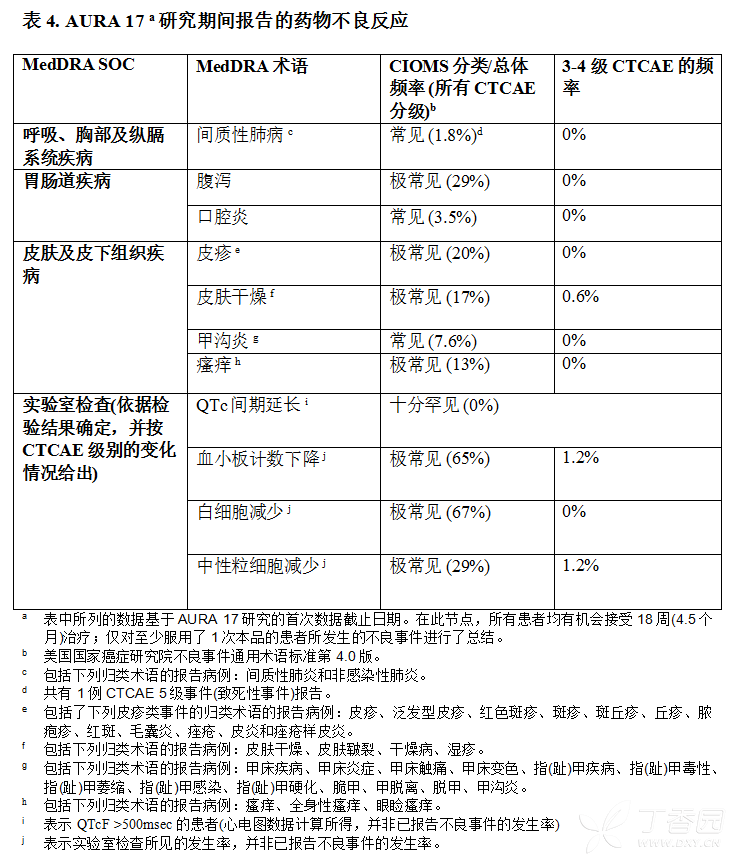
AURA17安全性数据总结*
在亚太地区II期研究(表4.AURA17,参见【临床试验】)中获得了171名(其中148名为中国患者)既往接受过治疗的T790M突变阳性的NSCLC患者使用本品的亚太人群安全性数据,这些患者服用的剂量为每日80mg。AURA17的安全性数据与全球II期安全性数据一致。绝大多数不良反应的严重程度为1或2级。
最常报告的ADR有:腹泻(29%)和皮疹(20%)。AURA17研究中,CTCAE3级以上不良事件的发生率为14%。在以每日80mg的方案接受本品治疗的患者中,因ADR减量的患者占0.6%。有1.2%的患者因为不良反应或实验室检查异常而提前停药。
特定药物不良反应的描述
间质性肺病(ILD)
II期研究期间,有6.2%的日本裔患者出现了ILD,而非日本裔亚裔患者和非亚裔患者的发生率分别为1.2%和2.4%。ILD或ILD样不良反应发生的中位时间为2.7个月(见【注意事项】)。
QTc间期延长
AURAex和AURA2研究的411名患者中,1名患者(0.2%)的QTc间期延长,并超过了500ms,有11名患者(2.7%)的QTc间期较基线值延长了60ms以上。对本品进行的一项药代动力学分析预测,QTc间期延长的发生率会出现浓度依赖性增加。AURAex或AURA2研究期间无心律失常事件报告(见【注意事项】)。
心肌收缩力改变
AURAex和AURA2研究中(N=411),具有基线和至少1次随访的LVEF评估的患者中2.4%(9/375)发生左心室射血分数(LVEF)下降>10%,且下降至<50%。
老年患者
在临床研究期间服用奥希替尼的患者中(N=411),有46%的年龄达65周岁或以上,有13%的年龄在75周岁或以上。和年龄较轻的受试者(<65岁)相比,年龄≥65岁的受试者出现导致研究药物剂量调整(暂停用药或减量)的不良反应的人数更多(23%vs.17%)。这两类患者。和年龄较轻的患者相比,老年患者出现的3级或以上的不良反应更多(32%vs.28%)。
可疑不良反应的报告
药品获得批准后,报告可疑不良反应非常重要。此举能够保证对产品的风险-获益平衡进行持续的监测。
对活性成分或任何辅料过敏。
本品不得与圣约翰草一起服用(见【药物相互作用】)。
EGFRT790M突变状态的评价
当考虑使用本品治疗局部晚期或转移性NSCLC时,首先需要明确EGFRT790M突变的状态。应采用经过充分验证的检测方法对采自组织样本的肿瘤DNA或血浆样本中获取的循环肿瘤DNA(ctDNA)进行检测。
在对肿瘤DNA(通过组织或血浆样本)的T790M突变状态进行检测时,必须使用稳健、可靠和敏感的检测方法。
通过组织或血浆检测后,如果T790M突变为阳性,则提示可使用本品治疗。然而,如果使用的是血浆ctDNA检测,且结果为阴性,则在可能的情况下应再进行组织检测,这是由于血浆检测可能会出现假阴性的结果。
间质性肺病(ILD)
在临床研究中,在使用本品的患者曾观察到重度、危及生命或致死性的间质性肺病(ILD)或ILD样的不良反应(如非感染性肺炎)。暂停用药后,上述绝大多数事件均会改善或缓解。临床研究中排除了既往存在ILD病史、药物诱导性ILD、需要类固醇激素治疗的放射性肺炎及临床存在活动性ILD证据的患者(见【不良反应】)。
临床研究期间,在接受本品治疗的1221名患者中,有2.9%的患者出现了间质性肺病(ILD)或ILD样的不良反应(如非感染性肺炎),其中有0.3%的受试者死亡。在两项II期研究期间,接受本品治疗的411名患者中有11名(2.7%)报告了ILD或ILD样不良反应,其中3或4级不良事件占0.7%,有1%的患者死亡。研究期间,有6.2%的日本裔患者出现了ILD,而亚裔患者和非亚裔患者的发生率分别为1.2%和2.4%(见【不良反应】)。
仔细检查出现肺部症状(呼吸困难、咳嗽、发热)急性发作和/或不明原因加重的患者,排除ILD。在对这些症状查找病因时,应暂停本品的用药。如果确诊为ILD,则应永久停用本品,并采取必要的治疗措施。
QTc间期延长
在服用本品的患者中出现过QTc间期延长。QTc间期延长可导致室性快速性心律失常(如尖端扭转型室性心动过速)或猝死的风险增加。AURAex或AURA2研究期间无心律失常事件报告(见【不良反应】)。通过静息心电图(ECG)检测,这两项研究排除了心脏节律或传导方面出现临床显著性异常的患者(如QTc间期>470ms)(见【不良反应】)。
如果可能,患有先天性长QT间期综合征的患者应避免使用本品。患有充血性心力衰竭、电解质异常或使用已知能够延长QTc间期的药物的患者应定期接受心电图(ECG)和电解质的监测。
至少两次独立心电图检测提示QTc间期>500ms的患者应暂时停用本品,直至QTc间期<481ms或恢复至基线水平(如基线QTc间期>=481ms),此时可恢复用药,但应按表1进行减量。合并出现QTc间期延长和下列任何一种情况的患者需永久停用本品:尖端扭转性室性心动过速、多形性室性心动过速、严重性心律失常的症状或体征。
心肌收缩力改变
AURAex和AURA2临床试验中,具有基线和至少1次随访的LVEF评估的接受奥希替尼治疗的患者中2.4%(9/375)发生左心室射血分数(LVEF)下降>10%,且下降至<50%。根据已有临床试验数据,尚不能确定心肌收缩力的改变与本品有因果关系。对于有已知心血管风险及存在可能影响LVEF情况的患者,需要考虑监测心脏功能,包括在基线和服药期间测定LVEF功能。对于本品治疗期间出现心脏事件相关症状和体征的患者,需要考虑心脏监测包括LVEF功能测定。
对驾驶及操纵机器能力的影响
本品对驾驶和操作机器能力无影响或影响轻微。
药代动力学相互作用
强效CYP3A4诱导剂可导致本品的暴露量下降。本品可能增加BCRP底物的暴露量。
可增加奥希替尼血浆浓度的活性物质
体外研究证实,本品主要通过CYP3A4和CYP3A5进行I期代谢。在临床药代动力学研究中,与200mg每日两次伊曲康唑(一种强效CYP3A4抑制剂)合并给药不会对本品的暴露量产生临床显著性影响(曲线下面积(AUC)增加24%,Cmax下降了20%)。因此,CYP3A4抑制剂不太可能对本品的暴露量产生影响。目前尚未确定其它对本品有催化作用的酶类。
可降低奥希替尼血浆浓度的活性物质
在临床药代动力学研究中,合并服用利福平(600mg每日1次,共21天)会使本品的稳态AUC下降78%。同样,代谢产物AZ5104的暴露量也有所下降,其AUC和Cmax分别下降了82%和78%。建议应避免同时使用本品和CYP3A4的强诱导剂(如苯妥英、利福平和卡马西平)。
CYP3A4的中度诱导剂(如波生坦、依法韦仑、依曲韦林和莫达非尼)也可降低本品的暴露量,因此应该慎用,如有可能也应避免使用。当奥希替尼与CYP3A的强诱导剂合并用药难以避免时,需要增加奥希替尼的剂量至每日160mg。停止服用CYP3A4的强诱导剂后三周,奥希替尼的剂量可恢复至每日80mg。本品禁止与圣约翰草合并使用(见【禁忌】)。
抑酸药物对奥希替尼的影响
在临床药代动力学研究中,合并给予奥美拉唑并不会对本品的暴露量产生临床相关性影响。本品可与改变胃内pH值的药物合并使用,无需任何限制。
服用奥希替尼后血浆浓度可能会被改变的其它活性物质
根据体外研究的结果,本品是BCRP转运蛋白的一种竞争性抑制剂。
在临床PK研究中,本品与瑞舒伐他汀(一种敏感的BCRP底物)合并使用后,后者的AUC和Cmax分别增加了35%和72%。服用本品时,如果患者合并服用了依赖BCRP进行分布且治疗指数较窄的药物,则应对其进行严密监测,以便及时发现因合并用药的暴露量增加而出现耐受性方面的变化。
(见【药代动力学】)。
在临床PK研究中,本品与辛伐他汀(一种敏感的CYP3A4底物)合并使用后,后者的AUC和Cmax分别增加了9%和23%。该变化很小,因此不太可能具有临床意义。
本品不太可能与CYP3A4的底物发生PK方面的相互作用。除CYP3A4外,我们未对受孕烷X受体(PXR)调控的其它酶的相互作用进行过研究。合并服用本品后,不能排除激素类避孕药暴露量下降的风险。
在全球范围进行了两项单臂、开放的临床研究,入组患有EGFRT790M突变阳性的非小细胞肺癌且既往全身治疗(包括一种EGFR-TKI)出现进展的患者,分别为AURAex(II期扩展队列(n=201))和AURA2(n=210)。
治疗前,所有患者都要求为经中心实验室EGFR突变检测为EGFRT790M突变阳性的NSCLC(研究中采用罗氏cobas确定肿瘤组织的T790M突变状态)。所有患者接受本品80mg每日一次的剂量。
这两项研究的主要疗效终点为基于盲态独立中心审核(BICR)根据RECISTv1.1评价的客观缓解率(ORR)。次要疗效终点包括:缓解持续时间(DoR)、疾病控制率(DCR)和无进展生存期(PFS)。
总体研究人群(AURAex和AURA2)的基线特征有:中位年龄63岁;13%的患者年龄≥75岁;女性(68%);白人(36%);亚洲人(60%)。所有患者均接受了至少一种既往治疗。31%的患者(N=129)既往接受过1种治疗(仅EGFR-TKI治疗),69%的患者(N=282)接受过2种或2种以上既往治疗。72%的患者从不吸烟,99%患者的世界卫生组织(WHO)体力状况评分为0或1分,39%的患者具有脑转移(稳定至少4周,且无需使用皮质类固醇激素治疗)。大多数患者(83%)在基线时已经出现了内脏转移。AURAex研究和AURA2研究的中位随访时间分别为6.9和6.7个月。
AURA研究(I期)是一项开放、单臂剂量递增和扩展的I期研究,其中多个剂量扩展组包括271名患有局部晚期或转移性NSCLC的经治患者。在63名经中心实验室检测EGFRT790M阳性的经治患者的扩展队列中研究了本品80mg每日一次的疗效和安全性。既往治疗包括EGFR-TKI和化疗。
该T790M阳性的研究人群(n=63)的人口学特征有:中位年龄60岁;女性(62%);白人(35%);亚洲人(59%);世界卫生组织(WHO)体力状况评分0或1的患者(100%);不吸烟者(67%)。
既往治疗线数范围从1线到9线。中位随访时间为8.2个月。表5总结了AURA研究及研究的汇总分析(AURAex和AURA2)的疗效。
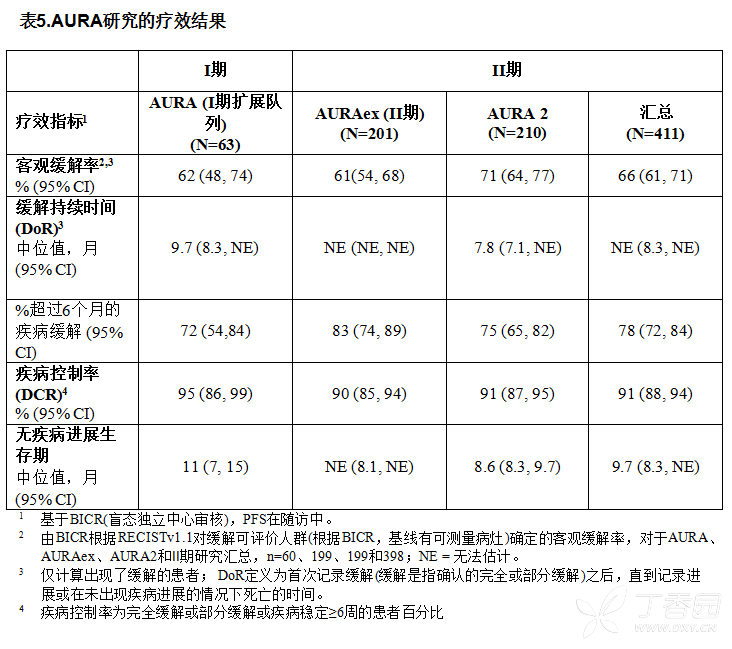
所有预先定义的亚组(治疗线数、种族、年龄和地区)分析中,客观缓解率都超过50%。
在总体人群中,86%(227/263例)在首次影像学扫描时(6周)出现了疾病缓解;96%(253/263例)在第2次影像学扫描时(12周)出现了疾病缓解。
在EGFRT790Mdenovo突变的患者中尚未进行临床研究。
AURA17(n=171)是一项II期、开放性、单臂研究,评估奥希替尼(80mg,口服,每日一次)在亚太地区确诊为局部晚期或转移性非小细胞肺癌(NSCLC)(IIIB-IV期)、具有EGFR敏感型基因突变(EGFRm)和EGFRT790M突变阳性、既往接受已批准的EGFR-TKI药物治疗后出现疾病进展的患者中的安全性和疗效。
在近期治疗时出现并证实疾病进展后,需要实施活检,以便中心实验室对EGFRT790M突变状态进行检测(研究中采用罗氏cobas确定肿瘤组织的T790M突变状态)。
本研究的有效性主要目的是盲态独立中心审核(BICR)通过RECIST1.1版本评估的客观缓解率(ORR)。有效性次要目的是评估缓解持续时间(DoR),疾病控制率(DCR)和无进展生存期(PFS)。
AURA17患者的基线特征如下:本研究中大部分患者为女性患者(117/171[68.4%]例)、亚洲患者(168/171[98.2%]例)和中国患者(148/171[86.5%]例)。研究入选时患者中位年龄为60.0岁(范围:26~82岁),≥50且<65岁年龄组患者比例最大(79/171[46.2%]例患者)。31.6%的患者(N=54)既往接受过1种治疗(仅EGFR-TKI治疗),68.4%的患者(N=117)接受过2种或2种以上既往治疗。大部分患者为转移性NSCLC(168/171[98.2%]例患者)、组织学类型腺癌(165/171[96.5%]例患者)并且WHO体力状况为1(145/171[84.8%]例患者)。
基于基线时靶病灶(TL)长径总和,试验开始时肿瘤负荷平均值为66.1mm(sd,33.55),且大部分患者基线TL大小为40至79mm(77/171[45.0%]例患者)。多数患者有内脏转移(141/171[82.5%]例患者)。中位随访时间为4.2个月。表6总结了AURA17研究的疗效。

遗传毒性:
奥希替尼Ames试验、小鼠淋巴瘤细胞试验、大鼠在体微核试验结果均为阴性。
生殖毒性:
动物研究显示,奥希替尼可能会损害雄性动物生育力。大鼠和犬给予奥希替尼1个月或更长时间,睾丸出现退行性变化,大鼠中的变化具有可逆性。
大鼠给予奥希替尼40mg/kg剂量约10周后,暴露量为人推荐剂量80mg下AUC的0.5倍时,未给药雌鼠与给药雄鼠交配后可见着床前丢失增加,提示雄鼠生育力下降。
根据动物研究结果,奥希替尼可能损害雌性动物生育力。重复给药毒性试验结果显示,大鼠给予奥希替尼达1个月或更长时间,当暴露量为人推荐剂量80mg下AUC的0.3倍时,观察到大鼠处于不动情期、卵巢中黄体退化以及子宫和阴道上皮细胞变薄等组织学变化。
给药1个月后卵巢变化的观测结果具有可逆性。雌性生育力研究显示,雌性大鼠于交配前两周至妊娠第8天给予奥希替尼20mg/kg/天(约为人推荐剂量80mg/天下Cmax的1.5倍),奥希替尼对雌鼠性周期及妊娠动物数未见影响,但可引起早期胚胎死亡。雌鼠停药后1个月再交配具有可逆性。
大鼠胚胎/胎仔发育毒性试验中,妊娠大鼠于胚胎着床前至器官发生结束后(妊娠第2~20天)给予奥希替尼20mg/kg/天(血浆暴露量约为临床暴露量的1.5倍),可见着床后丢失和胚胎早期死亡。
妊娠大鼠于着床到硬腭闭合期间(妊娠第6~16天)给予奥希替尼1mg/kg/天或更高剂量时(AUC值是人推荐剂量80mg时的0.1倍),与对照组相比,给药组胎儿畸形率和变异率可疑增加。
围产期毒性试验中,妊娠大鼠于器官发生至哺乳第6天给予奥希替尼30mg/kg/天,可见总窝仔流产和出生后死亡增加;20mg/kg/天剂量下可见出生时幼仔平均体重略微减少及出生后死亡增加,幼仔平均体重在哺乳期第4~6天开始增加。
致癌性:
目前尚未开展奥希替尼致癌性研究。